Lääketieteen asiantuntija
Uudet julkaisut
Sytomegalovirushepatiitti
Viimeksi tarkistettu: 05.07.2025

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Epidemiologia
CMV-infektio on laajalle levinnyt. 70–80 prosentilla aikuisista on veressään virusta neutraloivia vasta-aineita. Virusta erittyy virtsaan 4–5 prosentilla raskaana olevista naisista, kohdunkaulan kaapimissa sitä havaitaan 10 prosentilla naisista ja maidossa 5–15 prosentilla imettävistä äideistä. Eri syistä kuolleiden vastasyntyneiden keskuudessa yleistyneen CMV-infektion merkkejä havaitaan 5–15 prosentilla. Sytomegalovirushepatiitti muodostaa 1 prosentin virusperäisen akuutin ikterisen hepatiitin etiologisesta rakenteesta. Sytomegalovirushepatiitin esiintyvyyttä kokonaisuudessaan ei kuitenkaan ole tähän mennessä tutkittu.
CMV-infektion lähde on vain ihminen, sairas henkilö tai viruksen kantaja. Tartunta tapahtuu kosketuksessa, harvemmin ilmassa olevien pisaroiden ja enteraalisesti. Lisäksi infektio voi tapahtua parenteraalisesti, myös verensiirtojen aikana. Tämä tartuntareitti on ilmeisesti yleisempi kuin yleisesti uskotaan, minkä vahvistaa sytomegaloviruksen yleinen havaitseminen luovuttajilla (jopa 60 %). Infektion transplatsentaalinen tartuntareitti on luotettavasti todistettu. Sikiön tartunta tapahtuu äidiltä, joka on viruksen kantaja. Infektio välittyy suoraan istukan läpi tai synnytyksen aikana lapsen kulkiessa synnytyskanavan läpi. Vastasyntyneet voivat saada tartunnan äidinmaidon kautta.
Sytomegalovirushepatiitissa vallitsevat infektioreitit ovat ilmeisesti parenteraaliset ja perinataaliset, kun sytomegalovirus pääsee suoraan vereen ohittaen potilaan imukudoksen.
Syyt sytomegalovirushepatiitti
Sytomegalovirus, joka kuuluu Herpesviridae-heimoon, eristi vuonna 1956 M. Smith. Nykyisen luokittelun mukaan sitä kutsutaan ihmisen herpesvirustyypiksi 5 (HHV5). Tällä hetkellä tunnetaan kaksi sytomegaloviruksen serotyyppiä. Morfologisesti se on samanlainen kuin herpes simplex -virus. Virioni sisältää DNA:ta ja sen halkaisija on 120–140 nm, ja sitä viljellään hyvin ihmisalkion fibroblastiviljelmässä. Virus säilyy hyvin huoneenlämmössä ja on herkkä eetterille ja desinfiointiaineille. Sillä on heikko interferonogeeninen vaikutus. Sytomegalovirus aiheuttaa sairauksia yksinomaan ihmisillä. Sikiö ja vastasyntyneet ovat erityisen herkkiä virukselle.
Taudinaiheuttajia
Synnyssä
Sytomegalovirushepatiitin patogeneesi on edelleen epäselvä. Perinteisesti CMV:n uskotaan vaikuttavan ensisijaisesti sappiteihin kolestaattisen hepatiitin kehittyessä. CMV:n suora sytopaattinen vaikutus maksakudokseen on kuitenkin sallittu. Jotkut pitävät sytomegalovirusta epäilemättä maksan toimintaa edistävänä tekijänä. Tässä tapauksessa maksavaurioita voidaan havaita sekä synnynnäisessä että hankitussa CMV-infektiossa.
Sytomegalovirushepatiitissa esiintyvien yksittäisten maksasolujen vaurioiden muodostumisessa tärkeä rooli voi olla taudinaiheuttajan suoralla pääsyllä vereen (parenteraalinen infektiomekanismi). Tässä tapauksessa virus ei pääse imusuonistoon eikä siten alueellisiin imusolmukkeisiin, eikä varsinkaan lisäänny niissä. Taudinaiheuttaja ilmestyy välittömästi yleiseen verenkiertoon, josta se pääsee maksan parenkyymiin. Tätä patogeneettisen ketjun vaihetta voidaan kutsua tavanomaisesti parenkymaaliseksi diffuusioksi. Tässä tapauksessa virus voi tunkeutua välittömästi maksasoluihin, joissa se löytää lisääntymisolosuhteet.
Eristetyn sytomegalovirushepatiitin patogeneesissä ei voida sulkea pois eri sytomegalovirusgenotyyppien roolia eikä alttiilla yksilöillä kromosomissa 6 sijaitsevan HLA-järjestelmän (MHT) ehdokasgeenien polymorfismia.
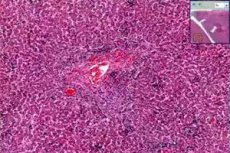
Patomorfologia
Terveillä aikuisilla esiintyvän akuutin sytomegalovirushepatiitin morfologisille muutoksille on ominaista intralobulaaristen granuloomien yhdistelmä, johon liittyy mononukleaaristen solujen sinusoidaalinen infiltraatio sekä periportaalinen tulehdus. Maksasolujen nekroosi voi olla lievää.
Immuunipuutteisilla aikuisilla (joille on tehty munuaisensiirto) kroonista sytomegalovirushepatiittia sairastavilla havaitaan periportaalista ja perisinusoidaalista fibroosia, sekasoluinfiltraatiota, maksasolujen pullistumaa ja kolestaasin merkkejä. Taudin varhaisvaiheissa sytomegalovirusantigeenejä havaitaan maksassa sinusoidaalisissa soluissa viruksen hematogeenisen leviämisen seurauksena. Havaitaan nekroottisia, dystrofisia muutoksia maksasoluissa, lymfosyyttistä infiltraatiota ja Kupfferin solujen aktivoitumista, kun taas spesifinen solutransformaatio on harvinaista. Sytomegalovirushepatiittiin näillä potilailla liittyy kolestaattinen oireyhtymä ja sappitiehyiden katoamisoireyhtymä. Tässä tapauksessa maksasoluissa havaitaan pp65-antigenemiaa ja CMV-DNA:ta, ja voidaan havaita maksakirroosin merkkejä.
Virushepatiitille tyypillisten klassisten muutosten lisäksi sytomegaloviruksen aiheuttamaa maksavauriota sairastavilla potilailla voi esiintyä pieniä neutrofiilisten polymorfonukleaaristen leukosyyttien aggregaatteja, jotka usein sijaitsevat infektoituneen maksasolun ympärillä ja joissa on CMV-inkluusiota. Immunohistokemialliset menetelmät ovat osoittaneet, että soluissa, joissa ei ole klassisia CMV-inkluusiota, sytoplasman basofiilinen rakeisuus johtuu sytomegalovirusmateriaalin läsnäolosta. Siten paitsi viruksen tuman sisäiset inkluusiot myös sytoplasman basofiilinen rakeisuus ovat tyypillinen merkki CMV-hepatiitista.
Yleisesti ottaen immuunipuutteisilla potilailla CMV-infektiolla on voimakkaampi sytopatogeeninen vaikutus ja se aiheuttaa laajempaa maksasolujen hajoamista kuin immuunipuutteisilla CMV-hepatiittia sairastavilla potilailla.
Synnynnäistä CMV-hepatiittia sairastavien lasten maksakudoksen morfologisille muutoksille on ominaista maksasolujen jättisolumuutos, kolestaasi, portaalifibroosi, sappitiehyiden epiteelin proliferaatio ja fulminanttien muotojen tapauksissa massiivinen maksanekroosi.
Oireet sytomegalovirushepatiitti
Sytomegalovirushepatiitti voi esiintyä sekä akuutissa että kroonisessa muodossa.
 [ 23 ]
[ 23 ]
Akuutti hankittu sytomegalovirushepatiitti
Hankittu akuutti CMV-hepatiitti lapsilla, nuorilla ja nuorilla aikuisilla voidaan diagnosoida tarttuvan mononukleoosin oireyhtymän osana. Joissakin tapauksissa havaitaan kuitenkin yksittäisiä maksavaurioita. Tässä tapauksessa tauti esiintyy anikterisenä, lievänä, keskivaikeana tai vaikeana. Yksittäisissä tapauksissa voi kehittyä fulminantti hepatiitti.
CMV-hepatiitin itämisaikaa ei ole tarkasti määritetty. Sen oletetaan olevan 2–3 kuukautta.
Preikterinen vaihe. Akuutin CMV-hepatiitin kliiniset oireet ja laboratorioarvot eivät olennaisesti eroa muiden etiologioiden aiheuttaman virushepatiitin oireista ja arvoista. Tauti alkaa vähitellen. Potilailla esiintyy ruokahaluttomuutta, heikkoutta, päänsärkyä ja vatsakipua. Joissakin tapauksissa ruumiinlämpö nousee 38 °C:seen.
Akuutin CMV-hepatiitti A:n esiikterisen vaiheen kesto vaihtelee yleensä 3–7 päivästä.
Preikterisen vaiheen kliiniset ilmentymät voivat olla poissa. Tällaisissa tapauksissa sytomegalovirushepatiitin ilmeinen alkumuoto alkaa keltaisuuden ilmaantuessa.
Keltatautijakso. Keltataudin puhkeamisen jälkeen potilailla esiintyvät keltatautia edeltävällä kaudella havaitut myrkytysoireet tai jopa pahenevat.
Akuutin sytomegalovirushepatiitin kliiniset ja laboratoriotutkimukset eivät olennaisesti eroa muiden etiologioiden virushepatiitin ilmentymistä.
Akuutin sytomegalovirushepatiitin ikterisen jakson kesto vaihtelee 13 - 28 päivän välillä.
Taudin jälkikarvaiselle jaksolle on ominaista potilaan hyvinvoinnin normalisoituminen, maksan ja pernan koon pieneneminen sekä entsyymiaktiivisuuden merkittävä väheneminen.
Krooninen sytomegalovirushepatiitti
Krooninen sytomegalovirushepatiitti kehittyy useimmiten immuunipuutteisilla potilailla (HIV-tartunnan saaneet, immunosuppressiivista hoitoa saavat, maksansiirron saaneet jne.). Siten sytomegalovirussiirteen vaurioita havaitaan 11–28,5 %:lla potilaista, joille on tehty maksansiirto eri syistä (autoimmuunimaksasairaudet, virushepatiitti jne.). CMV-DNA:ta havaitaan maksasoluissa 20 %:lla maksansiirron saaneista, joilla on kliininen, biokemiallinen ja histologinen kuva hepatiitista.
Kroonisen sytomegalovirushepatiitin kehittyminen on kuitenkin mahdollista myös immuunipuutteisilla lapsilla ja aikuisilla. Tässä tapauksessa krooninen hepatiitti voi kehittyä primaarisena kroonisena prosessina tai alun perin ilmenneen sytomegalovirushepatiitin seurauksena.
Hankittua kroonista CMV-hepatiittia sairastavien potilaiden kliiniset ja laboratorioarvot eivät eroa olennaisesti muiden etiologioiden aiheuttamassa kroonisessa virushepatiitissa havaituista.
Hankittua kroonista CMV-hepatiittia sairastavilla potilailla prosessin matala ja kohtalainen aktiivisuus on vallitsevaa. Lähes 3/4 tapauksista diagnosoidaan kohtalainen ja vaikea maksafibroosi.
Remissiovaiheen aikana myrkytysoireet kroonista CMV-hepatiittia sairastavilla potilailla ovat käytännössä poissa. Useimmilla potilailla maksan ulkopuoliset oireet häviävät. Maksan ja pernan koko pienenee, mutta niiden täydellistä normalisoitumista ei havaita. Yleensä maksan reuna työntyy kylkikaaren alta ulos enintään 1–2 cm. Perna palpoidaan alle 1 cm kylkikaaren reunan alapuolelta. Entsyymiaktiivisuus veressä ei ylitä normaaleja arvoja.
Hankitun sytomegalovirushepatiitin kliiniset ilmentymät vastaavat vaikeusasteeltaan vaihtelevan akuutin ja kroonisen virushepatiitin ilmentymiä. Kolmessa neljäsosassa hankitusta kroonisesta sytomegalovirushepatiitista diagnosoidaan keskivaikea ja vaikea maksafibroosi.
 [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
[ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ]
Synnynnäinen sytomegaloviruksen aiheuttama hepatiitti
Synnynnäinen CMV-infektio voi esiintyä sekä yleistyneessä muodossa, jolloin vaurioituu useita elimiä ja järjestelmiä, että paikallisesti, mukaan lukien maksa. Maksavaurio on tyypillistä synnynnäiselle CMV-infektiolle ja sitä esiintyy 40–63,3 %:lla potilaista. Maksamuutoksiin kuuluvat krooninen hepatiitti, kirroosi, sappitietulehdus ja intralobulaarinen kolestaasi. Myös ekstrahepaattisten sappiteiden vaurioita on raportoitu tulehduksesta atresiaan. Tähän mennessä sytomegaloviruksen rooli ekstrahepaattisten sappiteiden vaurioiden (atresia, kystat) synnyssä on edelleen epäselvä.
Synnynnäinen sytomegalovirushepatiitti rekisteröidään pääasiassa ensimmäisten elinkuukausien lapsilla, ja se etenee joko anikteerisessä muodossa, johon liittyy maksa-splenomegalia ja biokemiallinen aktiivisuus, tai ikteerisessä muodossa, johon liittyy keltaisuutta, tummaa virtsaa, maksa-splenomegaliaa, hypertransaminasemiaa, kohonneita alkalisen fosfataasin ja gamma-GT:n pitoisuuksia sekä maksakirroosin muodostumista puolella potilaista. Samaan aikaan synnynnäinen sytomegalovirushepatiitti voi edetä akuutissa ja pitkittyneessä muodossa, johon liittyy yksi- tai kaksiaaltoinen keltaisuus, lieviä myrkytysoireita, maksasoluentsyymien aktiivisuuden lisääntymistä 2-3 kertaa, kolestaattista oireyhtymää (1/3 potilaista), harvoin kroonisessa taudinkulussa, joka näissä tapauksissa kehittyy primaarisena kroonisena prosessina, joka ilmenee ilman keltaisuutta ja kohtalaisella tai korkealla patologisella aktiivisuudella.
 [ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
[ 31 ], [ 32 ], [ 33 ], [ 34 ], [ 35 ], [ 36 ], [ 37 ]
Synnynnäinen primaarinen krooninen sytomegalovirushepatiitti
Synnynnäistä kroonista CMV-hepatiittia sairastavilla lapsilla maksan patologisen prosessin minimaalinen aktiivisuus diagnosoidaan 1/4 tapauksista, alhainen aktiivisuus 1/3 tapauksista ja kohtalainen aktiivisuus 1/3 potilaista.
Prosessilla on voimakas fibroosia generoiva suunta. 1/3:lla potilaista diagnosoidaan voimakas fibroosi, 1/3:lla maksakirroosin merkkejä.
Synnynnäisen kroonisen CMV-hepatiitin kliiniset ilmentymät ja laboratorioparametrit eivät eroa perustavanlaatuisesti muiden etiologioiden virushepatiitista.
Remissiovaiheen aikana synnynnäistä kroonista CMV-hepatiittia sairastavilla potilailla myrkytysoireet ovat käytännössä poissa. Useimmilla lapsilla ekstrahepaattiset oireet häviävät. Maksan ja pernan koko pienenee, mutta niiden täydellistä normalisoitumista ei havaita. Yleensä maksan reuna työntyy kylkikaaren alta ulos enintään 1–2 cm. Perna palpoidaan useimmilla splenomegaliapotilailla alle 1 cm kylkikaaren reunan alapuolelta. Entsyymiaktiivisuus veressä ei ylitä normaaleja arvoja.
Sytomegalovirushepatiitti maksansiirtopotilailla
Sytomegalovirushepatiitti on yleisin CMV-infektion ilmentymä immunosuppressiivisen hoidon taustalla. Tällaisissa tapauksissa sytomegalovirushepatiitin diagnoosi tehdään maksaanibiopsian tulosten perusteella ja vahvistetaan virusviljelyllä, ppb5-antigeenillä, PCR:llä ja immunohistokemialla. Useimmille CMV-hepatiittipotilaista kehittyy erillinen maksavaurio, ja vain harvoille potilaille kehittyy yleistynyt CMV-infektio. Potilaille määrätään laskimonsisäinen gansikloviiri. AIDS:ssa sytomegalovirushepatiittia havaitaan 3–5 %:lla potilaista.
Ortotopisen maksansiirron läpikäyneillä ja AIDS-potilailla on mahdollista kehittää sytomegaloviruksen aiheuttaman ekstrahepaattisten sappiteiden ahtaumia, mikä vahvistetaan viruksen B havaitsemisella sappiteiden epiteelissä. Maksan luovuttajan ja vastaanottajan sytomegaloviruksen infektio ennen elinsiirtoa pidetään elinsiirron hyljintää edistävänä tekijänä.
 [ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
[ 41 ], [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ]
Sytomegaloviruksen aiheuttaman hepatiitin kulku
Taudin kulku voi olla akuutti (35 %) ja päättyä toipumiseen maksan toiminnallisen tilan täydelliseen palautumiseen 1–3 kuukauden kuluessa. 65 %:lla potilaista tauti muuttuu krooniseksi ilmeisen sytomegalovirushepatiitin seurauksena.
Mihin sattuu?
Diagnostiikka sytomegalovirushepatiitti
Sytomegalovirushepatiitti diagnosoidaan kliinisten, biokemiallisten ja serologisten tietojen yhdistelmän perusteella. Tauti alkaa yleensä astenodyspeptisillä oireilla: huonovointisuus, heikkous, ruokahaluttomuus, johon liittyy maksan koon kasvu ja hyperfermentemia. Potilaan anamneesissa voi olla viitteitä parenteraalisista manipulaatioista 2-3 kuukautta ennen nykyistä sairautta, eikä veren seerumissa ole hepatiittivirusten A, B, C, U, G jne. markkereita.
On tärkeää ottaa huomioon, että sytomegalovirushepatiitille on ominaista voimakas sytolyysioireyhtymä. Sen osoittamiseksi käytetään laajalti aminotransferaasiaktiivisuuden (ALAT, ASAT) ja LDH-fraktioiden (LDH-4, LDH-5) määritystä. Maksasolujen entsyymien lisääntynyt aktiivisuus on tyypillistä akuutille hepatiitille ja kroonisen sytomegalovirushepatiitin pahenemisvaiheelle. Maksasolujen entsyymien aktiivisuuden lisääntymisen aste sytomegalovirushepatiitin eri muodoissa vastaa muiden etiologioiden virushepatiitin lisääntymisen astetta.
Keltataudin läsnä ollessa on tärkeää määrittää kokonaisbilirubiinin taso ja konjugoituneiden ja konjugoimattomien fraktioiden suhde.
Maksan tulehdusprosessin aktiivisuus heijastuu jossain määrin veriseerumin proteiinispektrissä. Useimmissa tapauksissa kroonista CMV-hepatiittia sairastavilla potilailla veren seerumin kokonaisproteiinipitoisuus on normaali - 65-80 g/l. Potilailla, joilla on korkea aktiivisuus kroonisessa CMV-hepatiitissa, dysproteinemia muodostuu albumiinipitoisuuden laskun ja y-globuliinien ja -novien osuuden lisääntymisen vuoksi. Dysproteinemian luonne on kohtalainen ja saavuttaa merkittävän ilmentymän vain joillakin potilailla, kun albumiinipitoisuus laskee alle 45 %:iin ja y-globuliinipitoisuus ylittää 25 %:n.
Kroonisen sytomegalovirushepatiitin pahenemisvaiheessa proteiinisynteettisen toiminnan heikkeneminen on sitä merkittävämpää, mitä vakavampi maksan tulehdusprosessi on. Kroonista hepatiittia sairastavilla potilailla kehittyy eriasteisia veren hyytymisjärjestelmän häiriöitä (hypokoagulaatiota), jotka johtuvat pääasiassa maksan synteettisen toiminnan heikkenemisestä.
Akuutissa ja kroonisessa CMV-hepatiitissa maksan ultraäänikuva ei eroa muiden etiologioiden virushepatiitista.
Doppler-ultraäänimenetelmää käytetään veren virtauksen määrittämiseen porttilaskimojärjestelmässä ja portokavaalisten anastomoosien läsnäolossa, mikä mahdollistaa portaalihypertension diagnosoinnin, mukaan lukien sytomegaloviruksen etiologian maksakirroosia sairastavilla potilailla.
Morfologiset tutkimukset mahdollistavat objektiivisen arvioinnin maksan patologisen prosessin luonteesta, sen suunnasta ja toimivat myös yhtenä pakollisista kriteereistä hoidon tehokkuudelle.
Punktiobiopsian tuloksilla voi olla ratkaiseva erotusdiagnostinen arvo. Riittävän kokoisella maksapunktiolla saadulla morfologisella tiedolla on ratkaiseva merkitys kroonisen hepatiitin aktiivisuuden ja fibroosin asteen arvioinnissa sekä hoitotaktiikan valinnassa.
Mitä on tutkittava?
Kuka ottaa yhteyttä?
Hoito sytomegalovirushepatiitti
Gansikloviiria ja rekombinantti-interferoni A -valmisteita käytetään sytomegalovirushepatiitin hoitoon.
Alla on yhden kliinisen tutkimuksen tulokset, joissa hoidettiin 85 lasta, jotka saivat Viferon-hoitoa krooniseen sytomegalovirushepatiittiin. Heistä 31 lapsella oli hankittu ja 54:llä synnynnäinen CMV-hepatiitti. 49 lapsella synnynnäinen sytomegalovirushepatiitti yhdistettiin sappitiehyiden vaurioon (44:llä atresia ja 5:llä sappitiehyiden kystat) ja viidellä keskushermoston vaurioon.
Tarkkailtujen potilaiden joukossa oli 47 poikaa ja 38 tyttöä. Lasta oli alle 1-vuotiaita 55, 1–3-vuotiaita 23 ja yli 3-vuotiaita 7.
Kroonisen virushepatiitin aikana 45 lasta sai Viferon-monoterapiaa peräsuoliperäisinä peräpuikkoina, 31 lasta Viferonia yhdistettynä laskimonsisäisiin immunoglobuliineihin ja 9 lasta yhdistelmähoitoa, joka koostui Viferonista ja gansikloviirista. Interferonin annos on 5 miljoonaa/m² kolme kertaa viikossa.
Hoitojakson kesto oli 6 kuukautta 67 potilaalla, 9 kuukautta 11:llä ja 12 kuukautta 7 lapsella. Interferonihoidon tehokkuuskriteerit määritettiin EUROHEP-konsensuksen mukaisesti.
Kontrolliryhmään kuului 43 lasta. Siihen kuului 29 synnynnäistä ja 14 kroonista sytomegaloviruksen aiheuttamaa hepatiittia sairastavaa potilasta. Nämä lapset saivat perushoitoa, johon kuului vain kolereettisiä lääkkeitä, vitamiinivalmisteita ja maksansuojaimia.
Kliinisen ja biokemiallisen seurannan lisäksi sytomegaloviruksen replikatiivista aktiivisuutta varmistettiin taudin kulun aikana.
Kroonista CMV-hepatiittia sairastavien lasten osuus, jotka saavuttivat täydellisen remission viferonihoidon taustalla, oli pieni eikä saavuttanut 20 %:a. Kuitenkin jonkin verran remissiota saavuttaneiden lasten yhteenlaskettu ryhmä muodosti 78,8 % hoidetuista lapsista. Samaan aikaan remissiota ei saavutettu lähes 1/4:llä potilaista. On myös huomattava, että spontaania remissiota ei kehittynyt kenelläkään kontrolliryhmän lapsella saman ajan kuluessa.
Viferonihoidon tehokkuuden vertaileva analyysi synnynnäistä ja hankittua CMV-hepatiittia sairastavilla lapsilla osoitti, ettei viferonihoidon taustalla havaittu luotettavia eroja remission muodostumisprosentissa. P-arvot vaihtelivat välillä p>0,05 - p>0,2.
Vastatakseen kysymykseen sytomegalovirushepatiitin remission saavuttamisen tiheyden riippuvuudesta hoito-ohjelmasta, tunnistettiin kolme ryhmää. Ensimmäiseen kuuluivat potilaat, jotka saivat Viferon-monoterapiaa, toiseen lapset, jotka saivat Viferonia yhdessä laskimonsisäisten immunoglobuliinien kanssa, ja kolmanteen lapset, jotka saivat yhdistelmähoitoa Viferonin ja gansikloviirin kanssa.
Hoitotuloksissa ei havaittu merkittäviä eroja eri potilasryhmien välillä. Ainoastaan Viferon-hoitoa ja laskimonsisäisiä immunoglobuliineja saaneilla lapsilla havaittiin taipumus vähäisempään sytolyysin vaikeusasteeseen. P-arvot vaihtelivat välillä p > 0,05 - p > 0,1.
Samanlainen kuvio havaitaan myös arvioitaessa CMV:n replikatiivista aktiivisuutta kroonisessa sytomegalovirushepatiitissa lapsilla, jotka saivat erilaisia hoito-ohjelmia. CMV-DNA:n havaitsemisen tiheys dynaamisen havainnoinnin aikana oli käytännössä identtinen kaikkien kolmen ryhmän lapsilla. Vain hieman alhaisempi CMV:n replikatiivinen aktiivisuus havaittiin potilailla, joita hoidettiin Viferonilla yhdessä laskimonsisäisten immunoglobuliinien kanssa. P-arvot vaihtelivat välillä p > 0,05 - p > 0,2.
Lisätietoja hoidosta
Ennaltaehkäisy
CMV-infektion spesifistä ehkäisyä ei ole kehitetty. Kokeellista työtä rokotteen luomiseksi tehdään parhaillaan.
Epidemian vastaisia toimenpiteitä ei suoriteta infektiopesäkkeissä. Ottaen huomioon parenteraalisen infektiomekanismin mahdollisen roolin sytomegalovirushepatiitin muodostumisessa, toimenpiteet parenteraalisen infektion, myös verensiirron, kaikkien mahdollisuuksien estämiseksi näyttävät erityisen tärkeiltä. Kertakäyttöisten neulojen käyttö ja kirurgisten instrumenttien sterilointisääntöjen noudattaminen voivat estää infektion kokonaan parenteraalisten manipulaatioiden aikana.
Sytomegaloviruksen aiheuttaman infektion estämiseksi veren ja sen komponenttien verensiirroissa on tarpeen päättää luovuttajan veren CMV-DNA:n testaamisesta.

