Lisäkilpirauhaset
Viimeksi tarkistettu: 23.04.2024

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Vuonna 1879 ruotsalainen tiedemies S. Sandstrom kuvasi lisäkilpirauhaset ihmisillä ja antoi heille nimen. Lisäkilpirauhaset ovat tärkeitä elimiä. Heidän tehtävänsä on lisäkilpirauhashormonin (PTH) tuotanto ja erittyminen - yksi kalsiumin ja fosforin aineenvaihdunnan tärkeimmistä säätelijöistä.
Pariksi ylempi lisäkilpirauhasen (glândula parathyroidea superior) ja alempi lisäkilpirauhasen (glândula parathyroidea huonompi) - on pyöreä tai munan muotoisia vasikka sijoitettu takapinnalla kunkin lohkoa kilpirauhanen, yllä rauta, ja muut - pohja. Kunkin tiivisteen pituus on 4-8 mm, leveys - 3-4 mm, paksuus - 2-3 mm. Näiden rauhasien lukumäärä ei ole vakio ja voi vaihdella 2-7, keskimäärin neljä. Rauhojen kokonaismassa on keskimäärin 1,18 g.
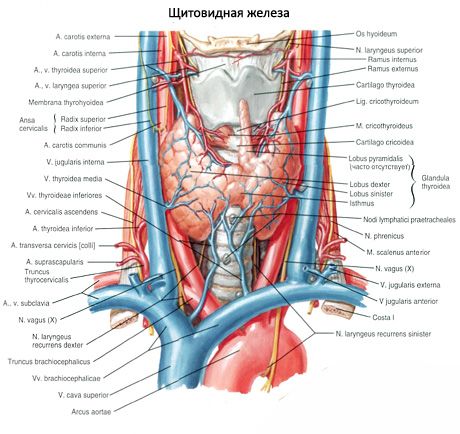
Lisäkilpirauhasen rauhaset poikkeavat kilpirauhasesta vaaleammalla värillä (lapsilla ne ovat vaaleanpunaisia, aikuisilla ne ovat kellertävän ruskeita). Usein lisäkilpirauhaset sijaitsevat alhaisen kilpirauhasen valtimoiden tai niiden oksojen kilpirauhasen tunkeutumispaikassa. Ympäröivistä kudoksista lisäkilpirauhaset erotetaan omalla kuitukapselilla, josta sidekudoskerrokset jättävät rauhaset. Viimeksi mainitut sisältävät suuren määrän verisuonia ja jakavat lisäkilpirauhaset epiteelisolujen ryhmiin.
Parenchyma-rauhaset muodostuvat pääasiallisista ja happofilisistä parathy- roytteistä, muodostaen säikeitä ja klustereita, joita ympäröivät ohuet sidekudoskuidut. Molempia solutyyppejä pidetään paratyloyrien kehityksen eri vaiheina. Pääparatyrosyytteillä on polyhedraalinen muoto, basofiilinen sytoplasma, jolla on suuri määrä ribosomeja. Näistä soluista erittyy tumma (aktiivisesti erittyy) ja valo (vähemmän aktiivinen). Acidophilic paratyrosyytit ovat suuria, selkeät ääriviivat sisältävät monia pieniä mitokondrioita glykogeenipartikkeleilla.
Lisäkilpirauhashormonin lisäkilpirauhashormoni (lisäkilpirauhashormoni), proteiinipitoinen hormoni, osallistuu fosfori-kalsiumin metabolian säätelyyn. Lisäkilpirauhashormoni vähentää kalsiumin vapautumista virtsassa, lisää imeytymistä suolistossa D-vitamiinin läsnäollessa. Lisäkilpirauhashormonin antagonisti on thyrecalcitonin.
Lisäkilpirauhasen embryogeneesi
Lisäkilpirauhanen kehittyy parittujen III- ja IV-taskujen epiteelistä. Kehityksen seitsemännessä viikossa korpussien epiteeliset alkuosat erosivat taskutasojen seinistä ja kasautumisprosessissa sekoittuvat kaula-suuntaan. Tulevaisuudessa lisäkilpirauhaset muodostavat pysyvän asennon kilpirauhasen oikean ja vasemman lonkan takapintoihin.
 [7], [8], [9], [10], [11], [12],
[7], [8], [9], [10], [11], [12],
Lisäkilpirauhasen alukset ja hermot
Lisäkilpirauhasen verenkiertoa hoidetaan ylä- ja alahygienivelen oksilla sekä ruokatorven ja henkitorven oksilla. Laskimoverilä virtaa pitkin samaa nenäa. Lisäkilpirauhasen turvotus on samanlainen kuin kilpirauhan innervaatio.
Lisäkilpirauhasen ikäominaisuudet
Lisäkilpirauhasen kokonaismäärä vastasyntyneessä vaihtelee 6-9 mg: n välillä. Ensimmäisen elinvuoden aikana niiden kokonaismassa kasvaa 3-4 kertaa, 5-vuotiaana kaksinkertaistuu ja 10 vuoden kolminkertaistuu. 20 vuoden kuluttua neljän lisäkilpirauhasen kokonaismassa on 120-140 mg ja pysyy vakiona vanhuuteen asti. Kaikissa ikäkausina naisten lisäkilpirauhasen massa on hieman suurempi kuin miesten.
Yleensä miehellä on kaksi paria kilpirauhasen (ylempi ja alempi), jotka sijaitsevat kilpirauhasen takapinnalla kapselin ulkopuolella, lähellä ylä- ja alapylväitä. Lisäkilpirauhasen määrä ja sijainti voivat kuitenkin vaihdella; joskus jopa 12 lisäkilpirauhasta löydetään. Ne voivat sijaita kudoksissa kilpirauhasen ja kateenkorvassa, etu- ja taka välikarsinassa, sydänpussin, ruokatorven takana alueella kaulavaltimon kaksijakoisuus. Yläosien lisäkilpirauhaset ovat litteän munanmuotoiset, alemmat pallomaiset. Niiden koko on noin 6x3 - 4x1,5 - 3 mm, kokonaismassa 0,05-0,5 g, väri on punertava tai kellertävä ruskea. Lisäkilpirauhasen verenkiertoa harjoittavat pääasiassa alemman kilpirauhasen oksat, laskimonsuojaus tapahtuu kilpirauhasen, ruokatorven ja henkitorven kautta. Lisäkilpirauhaset ovat sympaattisia toistuvien ja ylemmän kurkunpään hermojen sympaattisten kuitujen kanssa, parasympaattinen innervaatio suoritetaan vagus-hermoja. Lisäkilpirauhaset peitetään ohuella sidekudoskapselilla; Erilaiset väliseinät tunkeutuvat rauhasisiin. Ne sisältävät verisuonia ja hermokuituja. Lisäkilpirauhasen parenkyymi koostuu parathyreosyytteistä tai suurista soluista, joista värikkyysaste erottaa hormonaalista aktiivista valoa tai kiiltävää sekä lepäävät tummat solut. Pääsolut muodostavat klustereita, säikeitä ja klustereita, ja vanhuksilla - ja follicleillä kolloidia ontelossa. Aikuisilla solut esiintyvät lähinnä lisäkilpirauhanen reunoilla, jotka on värjätty eosiini-, eosinofiiliset tai oksifilisillä soluilla, jotka ovat degeneraa- tuvia pääseoksia. Lisäkilpirauhasessa voi esiintyä siirtymämuotoja myös tärkeimpien ja oksifisten solujen välillä.
Ensimmäinen onnistumisten tarkentavia kysymyksiä synteesissä, dekoodaamiseksi rakenteet tutkimuksessa PTH-vaihto saavutettiin sen jälkeen, kun 1972 .. Lisäkilpirauhashormoni - on yksiketjuinen polypeptidi, joka koostuu 84 aminohappotähteestä vailla kysteiiniä, jonka molekyylipaino on noin 9500 daltonia, valmistetaan lisäkilpirauhaset alkaen bioprekursori - proparatgormona (proPTG), jossa on 6 ylimääräistä aminohappoa NH 2 -kontse. ProPTG syntetisoitu tärkein soluissa lisäkilpirauhasten (niiden rakeinen endoplasmakalvostossa) ja aikana proteolyyttistä hajoamista Golgin laitteessa muuttuu lisäkilpirauhashormonia. Sen biologinen aktiivisuus on huomattavasti pienempi kuin PTH: n. Ilmeisesti, proPTG veressä terveiden ihmistä kateissa, mutta patologisissa tiloissa (adenooma lisäkilpirauhasten), se voidaan erittyy vereen yhdessä PTH. Äskettäin edeltäjä proPTG keksittiin - preproPTG sisältää lisäksi 25 aminohappotähdettä NH2-terminuksessa. Näin preproPTG sisältää 115 aminohappotähdettä proPTG - 90 ja PTH - 84.
Nyt naudan ja sian kilpirauhashormonin rakenne on täysin vakiintunut. Lisäkilpirauhasten adenoomista on eristetty kilpirauhashormoni, mutta sen rakenne on vain osittain purettu. Eri lisäkilpirauhashormonin rakenteessa on eroja, mutta eläinten ja ihmisten parathormoneilla on ristireaktiivisuus. Ensimmäisestä 34 aminohappotähteestä koostuva polypeptidi käytännössä säilyttää luonnollisen hormonin biologisen aktiivisuuden. Tämä antaa meille mahdollisuuden olettaa, että jäljelle jäävä lähes prosenttimäärä molekyylistä karboksyylipäässä ei ole suoraan riippuvainen lisäkilpirauhashormonin päävaikutuksista. Lisäksi lisämunuaisten hormonin biologinen ja immunologinen aktiivisuus esitetään myös 1-29-kertaisella fragmentilla. Immunologista vaikutusta omaavat myös biologisesti inaktiivinen fragmentti 53-84, eli nämä parathormonin ominaisuudet osoittavat ainakin 2 osaa sen molekyylistä.
Kiertävä lisäkilpirauhashormonin veressä on heterogeeninen, se eroaa lisäkilpirauhasen erittämästä alkuperäisestä hormonista. Veressä on vähintään kolme eri tyyppistä lisäkilpirauhashormonia: ehjä lisäkilpirauhashormoni, jonka molekyylipaino on 9500 daltonia; biologisesti inaktiiviset aineet lisäkilpirauhashormonimolekyylin karboksyyliosasta, jonka molekyylipaino on 7000-7500 daltonia; biologisesti aktiivisia aineita, joiden molekyylipaino on noin 4000 daltonia.
Jopa pienempiä fragmentteja löydettiin laskimoverestä, mikä osoittaa niiden muodostumisen periferiassa. Pääelimet, joissa lisäkilpirauhashormonin fragmentteja muodostuu, ovat maksa ja munuaiset. Lisäkilpirauhashormonin fragmentoituminen näissä elimissä lisääntyy maksapatologialla ja kroonisella munuaisten vajaatoiminnalla (CRF). Näissä olosuhteissa lisäkilpirauhashormonin fragmentit pysyvät verenkiertoon paljon kauemmin kuin terveillä ihmisillä. Maksa imee pääasiallisesti ehjää lisäkilpirauhashormonia, mutta ei poista verestä joko lisäkilpirauhashormonin karboksyyliterminaalia tai aminoterminaalisia fragmentteja. Eturauhasen hormonien aineenvaihdunnassa on johtava rooli munuaisissa. Ne muodostavat lähes 60% karboksiterminaalisen immunoreaktiivisen hormonin metabolisesta puhdistumasta ja 45% lisäkilpirauhashormonin aminoterminaalisesta fragmentista. Lisäkilpirauhashormonin aktiivisen aminoterminaalisen fragmentin pääasiallinen aineenvaihdunta-alue on luut.
Lisätty lisäkilpirauhashormonin pulssierottelu, joka oli voimakkain yöllä, havaittiin. 3-4 tunnin kuluttua yöunen alusta, sen sisältö veressä on 2,5-3 kertaa suurempi kuin keskimääräinen päivittäinen taso.
Ensisijainen tehtävä PTH on ylläpitää kalsiumin homeostaasiin. Kuitenkin, seerumin kalsium (kokonais- ja ionisoitu erityisesti) on tärkein säätelijä eritystä lisäkilpirauhashormonin (väheneminen kalsiumin stimuloi lisäkilpirauhashormonin erittymistä, kasvava - vaimentaa), eli asetus suoritetaan palautteen periaate ... Parannettu konversio-olosuhteissa hypokalsemia proPTG PTH. Vapauttamista Lisäkilpirauhashormonin on tärkeä rooli veren magnesiumpitoisuus (kohonneet stimuloi ja alhainen - estää lisäkilpirauhashormonin eritys). Kohderyhminä ovat lisäkilpirauhashormonin munuaiset, ja luut luuranko, mutta tiedämme vaikutus lisäkilpirauhashormonin kalsiumin imeytymistä suolistossa, toleranssi hiilihydraattien, lipidien veren seerumin, sen rooli kehityksen impotenssi, kutinaa ja niin edelleen. D.
Jotta luustettaisiin lisäkilpirauhashormonin vaikutuksesta luuhun, on tärkeää antaa lyhyt informaatio luukudoksen rakenteesta, sen fysiologisen resorption ja remodelingin erityispiirteistä.
Tiedetään, että suurin osa elimistössä olevasta kalsiumista (korkeintaan 99%) on luukudoksessa. Koska fosfori-kalsiumyhdisteiden luu on luu, myös luiden sisältämässä osassa fosforin kokonaispitoisuutta. Heidän kudoksensa, huolimatta näennäisestä staattisesta, on jatkuvasti remodeled, aktiivisesti vascularized ja on korkeat mekaaniset ominaisuudet. Luu on fosforin, magnesiumin ja muiden yhdisteiden dynaaminen "depot", joka on välttämätön homeostaasin ylläpitämiseksi mineraalien aineenvaihdunnassa. Sen rakenne sisältää tiheitä mineraalikomponentteja, jotka ovat läheisessä yhteydessä orgaaniseen matriisiin, joka koostuu 90-95% kollageenista, pienistä määristä mukopolysakkarideja ja ei-kollageeniproteiineja. Luun mineraalinen osa koostuu hydroksiapatiitista - sen empiirinen kaava on Ca10 (PO4) 6 (OH) 2- ja amorfinen kalsiumfosfaatti.
Luu muodostaa ei-erilaistetuista mesenkymaalisista soluista peräisin olevat osteoblasit. Nämä ovat mononukleaarisia soluja, jotka liittyvät luun orgaanisen matriisin komponenttien synteesiin. Ne sijaitsevat yksikerroksisessa luupinnalla ja ovat tiiviissä yhteydessä osteoidiin. Osteoblastit ovat vastuussa osteoidin laskeumasta ja sen myöhemmästä mineralisaatiosta. Elämänsä tuote on alkalinen fosfataasi, jonka sisältö veressä on epäsuora indikaattori niiden toiminnasta. Ympäröi mineralisoidaan osteidom, jotkut osteoblastit tullut osteosyyttejä - mononukleaarisolut, sytoplasmassa, joka muodostaa kanavat, jotka liittyvät viereiseen tubulukset osteosyyttien. He eivät osallistu luun remontointiin, vaan osallistuvat perilakuutiotuhon prosessiin, joka on tärkeä seerumin kalsiumpitoisuuden nopean säätelyn kannalta. Luun resorptiota tekevät osteoklasit - jättiläiset polynuklearmeja, jotka ilmeisesti muodostuvat mononukleaaristen makrofagien fuusioitumisesta. Oletetaan myös, että osteoklastien prekursorit voivat olla luuytimen hematopoieettisia kantasoluja. Ne ovat liikkuvia, muodostavat luun kanssa kosketuksessa olevan kerroksen, joka sijaitsee sen suurimman resorption alueella. Vapautumisen takia proteolyyttisten entsyymien ja happaman fosfataasin osteoklastien aiheuttaa kollageenin hajoamista, hydroksiapatiitti jakautuminen ja erittymistä mineraalien matriisissa. Hiljattain muodostunut hieman mineralisoitu luukudos (osteoidi) on resistenttejä osteoklastiseen resorptiota kohtaan. Osteoblastien ja osteoklastien toiminnot ovat riippumattomia, mutta keskenään johdonmukaisia, mikä johtaa luuston normaaliin remontointiin. Luun kasvun pituus riippuu enchondralin luutumista, kasvun leveydestä ja sen paksuudesta - periostealisesta luutumista. 47 Ca: n kliiniset tutkimukset osoittivat, että päivittäin jopa 18% koko kalsiumpitoisuudesta päivitetään. Jos luut ovat vahingoittuneet (murtumat, infektioprosessit), reseksoitu luu resorboituu ja uusi luu muodostuu.
Solujen komplekseja, jotka osallistuvat paikalliseen luun resorptioprosessiin ja luun muodostumiseen, kutsutaan perustaksi monisoluisia yksikköjä (BMI - Basic multicellular unit). Ne säätelevät kalsiumin, fosforin ja muiden ionien paikallista konsentraatiota, luun orgaanisten komponenttien synteesiä, erityisesti kollageenia, sen organisointia ja mineralisaatiota.
Lisäkilpirauhashormonin pääasiallinen toiminta luuran luissa on resorptioprosessien tehostaminen, joka vaikuttaa sekä luun rakenteen mineraali- että orgaanisiin komponentteihin. Lisäkilpirauhashormoni edistää osteoklastien ja niiden aktiivisuuden kasvua, johon liittyy lisääntynyt osteolyyttinen vaikutus ja luun resorption lisääntyminen. Tämä liuottaa hydroksiapatiitin kiteet kalsiumin ja fosforin vapautumiseen verenkiertoon. Tämä prosessi on tärkein mekanismi kalsiumin määrän lisäämiseksi veressä. Se koostuu kolmesta osasta: kalsiumin mobilisointi perilakunaarisesta luusta (syvät osteosyytit); osteo-esiastesolujen proliferaatio osteoklasteissa; ylläpitää kalsiumin vakiotasoa veressä säätämällä sen vapautumista luusta (pinnalliset osteosyytit).
Siten, lisäkilpirauhashormoni aluksi lisää aktiivisuutta osteoklastien ja osteosyytit, vahvistaa osteolyysiä, aiheuttaen nousun veren kalsiumpitoisuus ja lisääntynyt hydroksiproliinin erittymistä virtsaan ja sen. Tämä on lisäkilpirauhashormonin ensimmäinen, laadullinen, nopea vaikutus. Toisen vaikutuksen lisäkilpirauhashormonin vaikutuksesta luuhun on kvantitatiivinen. Se liittyy osteoklastien altaan lisääntymiseen. Aktiivisella osteolyysillä on ärsyke lisääntyneelle osteoblastien lisääntymiselle ja aktivoituu resorption ja resorption pääasiallinen resorptio ja muotoilu. Liian lisäkilpirauhashormonilla esiintyy negatiivista luuston tasapainoa. Tämä liittyy liialliseen vapautumiseen hydroksiproliinin - kollageenin hajoamistuote, ja siaalihappo, mukopolysakkaridit sisältyy rakenteeseen. Lisäkilpirauhashormoni aktivoi syklisen adenosiinimonofosfaatin (cAMP). CAMP: n erittyminen virtsassa lisäkilpirauhashormonin antamisen jälkeen voi toimia osoituksena kudosherkkyydestä siihen.
Lisäkilpirauhashormonin tärkein vaikutus munuaiseen on sen kyky vähentää fosforin reabsorptiota lisäämällä fosfatiaa. Mekanismi vähentäminen eri puolilla nephron on erilainen: proksimaalisessa osassa tämä vaikutus johtuu kasvu lisäkilpirauhashormonin läpäisevyys ja tapahtuu osallistumisen cAMP distaalisen - on riippumaton cAMP. Lisäkilpirauhashormonin fosfaturoiva vaikutus muuttuu D-vitamiinin puutoksella, metabolisella asidoosilla ja fosforipitoisuuden vähenemisellä. Lisäkilpirauhashormonit lisäävät hieman kalsiumin koko putkimainen reabsorptiota. Samalla se pienentää sitä proksimaalisesti ja lisää sitä distaalisissa osissa. Viimeksi mainitulla on määräävä rooli - lisäkilpirauhashormoni vähentää kalsiumin puhdistumista. Lisäkilpirauhashormoni vähentää natriumin ja sen bikarbonaatin putkimainen reabsorptiota, mikä selittää asidoosin lisääntymisen hyperparatyreoosissa. Se lisää muodostumista munuaisten dioksiholekaltsiferola 1,25-1,25 (OH 2 ) D 3 - aktiivinen-vitamiinin 3. Tämä yhdiste lisää kalsiumin reabsorptiota ohutsuolessa stimuloimalla tietty kalsiumia sitovaa proteiinia (Ca-sitova proteiini, CaBP) sen seinämään.
Lisäkilpirauhashormonin normaali taso on keskimäärin 0,15-0,6 ng / ml. Se vaihtelee iän ja sukupuolen mukaan. Lisäkilpirauhashormonin keskimääräinen määrä veressä 20-29-vuotiailla (0,245 ± 0,017) ng / ml, 80-89 vuotta - (0,545 ± 0,048) ng / ml; lisäkilpirauhashormonin taso 70-vuotiailla naisilla - (0,728 ± 0,051) ng / ml samassa iässä oleville miehille - (0,466 ± 0,40) ng / ml. Näin ollen lisäkilpirauhashormonin sisältö kasvaa iän myötä, mutta enemmän naisilla.
Yleensä hyperkalsemian erilai- sen diagnoosin yhteydessä on käytettävä useita erilaisia testejä.
Esittelemme luokittelun OV Nikolaevin ja VN Tarkaevan (1974) luokittelun pohjalta laaditun kliinisen patogeenisen luokituksen perusteella.
Kliinis- patogeneettinen luokittelu sairauksiin, jotka liittyvät paratyroidihormonien heikentyneeseen erittymiseen ja sen herkkyyteen
Primaarinen hyperparatyreoosi
- Patogeneesillä:
- hyperfunktio adenoma (adenoomat);
- liikakasvu OGZHZH;
- kilpirauhasen rakkuloiden hyperfunktio;
- tyypin I endokriininen munuaisten vajaatoiminta hyperparatyreoosi (Vermeerin oireyhtymä);
- tyypin II endokriininen munuaisten vajaatoiminta ja hyperparatyreoosi (Sipplen oireyhtymä).
- Kliiniset ominaisuudet:
- luun muoto:
- osteoporoosi
- fibro-kystinen osteitis,
- "Pagetoid";
- visceropaattinen muoto:
- jossa munuaisten, maha-suolikanavan, neuropsykoottisen pallon;
- sekamuotoisena.
- luun muoto:
- Down stream:
- akuutti;
- krooninen.
Toissijainen hyperparatyreoosi (sekundaarinen hyperfunktio ja lisäkilpirauhasen hyperplasia, joilla on pitkittynyt hypokalsemia ja hyperfosfatemia)
- Munuaispatologia:
- krooninen munuaisten vajaatoiminta;
- tubulopatia (kuten Albright-Fanconi);
- munuaissyöpät.
- Suolen patologia:
- oireyhtymä heikentynyt suolen imeytyminen.
- Luunpatologia:
- osteomalasia-seniili;
- puerperal;
- idiopaticheskaya;
- Pagetin tauti.
- D-vitamiinin riittämättömyys:
- munuaissairaus;
- maksa;
- perinnölliset entsyymiopatiat.
- Malignantit sairaudet: myelooma.
hyperparatyreoosi tertiäärinen
- Autonomisesti toimiva adenoma (adenoma) lisäkilpirauhasen rauhasista, kehittyy pitkäaikaisen sekundaarisen hyperparatyreoosin takia.
Psevdogiperparatireoz
- Lisäkilpirauhashormonin tuotanto ei-paratiikaryhmän kasvaimista.
Lisäkilpirauhasen hormonitoimiset kystiset ja kasvainmuodostukset
- Kystti.
- Hormonaaliset inaktiiviset kasvaimet tai karsinooma.
Gipoparatireoz
- Synnynnäinen epätasapaino tai lisäkilpirauhasen vajaatoiminta.
- Idiopaattinen, autoimmuuninen genesi.
- Postoperatiivinen, kehitetty lisäkilpirauhasen poistamisen yhteydessä.
- Postoperatiivinen verenkierron heikkenemisen ja innervaation vuoksi.
- Säteilyvahingot, eksogeeniset ja endogeeniset (kauko sädehoito, kilpirauhasen käsittely radioaktiivisella jodilla).
- Vaurio lisäkilpirauhaset, joilla on verenvuoto, infarkti.
- Tarttuva vaurio.
Pseudohypoparathyreosis
- I - kohde - elinten tyyppinen herkkyys lisäkilpirauhashormoonille, joka riippuu adenylaattisyklaasista;
- Tyyppi II on kohde-elinten herkkyys lisäkilpirauhashormonille riippumatta adenylaattisyklaasista, mahdollisesti autoimmuunisynteesistä.
Pseudo pseudohypyparatyroosi
Pseudohypoparatireoidimyrkyn somaattisten oireiden esiintyminen terveillä sukulaisilla potilailla, joilla on pseudohypoparatireoidi, ilman ominaispiirteitä biokemiallisia häiriöitä ja ilman tetanystä.

