Neuroleptit tai antipsykootit
Last reviewed: 24.06.2018

Meillä on tiukat lähdekoodin valintaohjeet ja linkitämme vain hyvämaineisiin lääketieteellisiin sivustoihin, akateemisiin tutkimuslaitoksiin ja aina kun mahdollista lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa olevat numerot ([1], [2] jne.) ovat klikattavia linkkejä näihin tutkimuksiin.
Jos mielestäsi jokin sisällöstämme on epätarkkaa, vanhentunutta tai muuten kyseenalaista, valitse se ja paina Ctrl + Enter.
Antipsykootit (neuroleptit) ovat psykotrooppisten lääkkeiden luokka, joita käytetään pääasiassa skitsofrenian hoitoon. Tällä hetkellä on yleistä erottaa kaksi lääkeryhmää (tai -luokkaa): tyypilliset ja epätyypilliset antipsykootit. Alla on tietoa kunkin lääkeryhmän farmakologisista ominaisuuksista, käyttöaiheista ja hoidon sivuvaikutuksista.
Tyypillisten antipsykoottien käyttöaiheet
Tällä hetkellä perinteisten neuroleptien määräämisen tärkeimmät käyttöaiheet psykofarmakoterapian alan arvovaltaisten tutkijoiden suositusten mukaan ovat seuraavat.
- Lievittää vakavien psykoottisten oireiden aiheuttamia psykomotorisia agitaatio- ja käyttäytymishäiriöitä. Näissä tapauksissa on osoitettu, että käytetään suun kautta tai parenteraalisesti otettavia antipsykoottisia lääkkeitä, sekä globaaleja (klopromatsiini, levomepromatsiini, tioproperatsiini, zuklopentiksoliini) että selektiivisiä - hallusinatorisiin ja paranoidisiin häiriöihin vaikuttavia aineita (haloperidoli, trifluoperatsiini).
- Relapsien ehkäisyyn tarkoitettu hoito. Tätä tarkoitusta varten määrätään depotmuotoisia lääkkeitä, erityisesti potilaille, joilla on huono lääkemyöntyvyyden tunne (haloperidolidekanoaatti, flupentiksolin pitkäaikainen muoto), tai pieniä tai keskisuuria lääkeannoksia disinhibitorisen (antinegatiivisen) vaikutuksen saavuttamiseksi niistä lääkkeistä, joiden suuria annoksia käytetään akuuttien psykoottisten häiriöiden lievittämiseen (flupentiksoli, zuklopentiksoli). Tällaisessa hoidossa suositellaan myös niin sanottujen pienten neuroleptien (tioridatsiini, klooriprotikseeni, sulpiridi) määräämistä, joiden psykotrooppinen vaikutus koostuu vaikutuksesta masennusoireiden ja unettomuushäiriöiden ilmenemismuotoihin.
- Atyyppisten antipsykoottisten lääkkeiden terapeuttisen resistenssin voittaminen akuuttien psykoottisten tilojen hoidossa. Tähän tarkoitukseen käytetään yleensä perinteisten antipsykoottien parenteraalisia muotoja, joilla on globaali (klooripromatsiini, levomepromatsiini jne.) ja selektiivinen (haloperidoli) antipsykoottinen vaikutus.
Nämä lääkkeet aiheuttavat erilaisia sivuvaikutuksia, joiden luonne riippuu kunkin lääkkeen farmakologisen profiilin ominaisuuksista. Antipsykootit, joilla on voimakkaampi kolinolyyttinen vaikutus, aiheuttavat useammin akkommodaatiohäiriöitä, ummetusta, suun kuivumista ja virtsaumpea. Sedatiivinen vaikutus on tyypillisempi antipsykooteille, joilla on voimakas antihistamiinivaikutus, ja ortostaattinen hypotensio on tyypillisempi lääkkeille, jotka salpaavat a1-adrenergisiä reseptoreita. Tyypillisten neuroleptien aiheuttama kolinergisen, noradrenergisen ja dopaminergisen signaloinnin esto voi johtaa lukuisiin seksuaalisen alueen häiriöihin, kuten amenorreaan tai dysmenorreaan, anorgasmiaan, galaktorreaan, rintojen turvotukseen ja arkuuteen sekä potenssin heikkenemiseen. Seksuaalisen alueen sivuvaikutukset liittyvät pääasiassa näiden lääkkeiden kolinolyyttisiin ja adrenoblokkeriominaisuuksiin sekä prolaktiinin erityksen lisääntymiseen dopamiinin aineenvaihdunnan estymisen vuoksi. Tyypillisten neuroleptien vakavimmat sivuvaikutukset ovat motoriset toimintahäiriöt. Ne ovat yleisin syy potilaiden lopettaa lääkkeiden käyttö. Kolme pääasiallista hoidon sivuvaikutusta, jotka liittyvät motoriseen sfääriin, ovat varhaiset ekstrapyramidaalioireyhtymät, tardiivi dyskinesia ja maligni neuroleptioireyhtymä.
Ekstrapyramidaalisten oireyhtymien uskotaan liittyvän D2-reseptorien salpautumiseen tyvitumakkeissa. Näitä ovat dystonia, neuroleptiparkinsonismi ja akatisia. Akuutin dystonisen reaktion (varhaisen dyskinesian) ilmenemismuotoja ovat äkillisesti kehittyvä hyperkinesia, okulogyyriset kriisit, kasvojen ja vartalon lihasten supistukset sekä opisthotonus. Nämä häiriöt ovat annoksesta riippuvaisia ja ilmenevät usein 2–5 päivän kuluttua hoidon aloittamisesta erittäin tehokkailla neurolepteillä, kuten haloperidolilla ja flufenatsiinilla. Varhaisen dyskinesian lievittämiseksi neuroleptiannosta pienennetään ja määrätään antikolinergisiä lääkkeitä (biperideeni, triheksifenidyyli). Tardiivi dyskinesia vaikuttaa yleensä niskalihaksiin, ja toisin kuin akuutti dystoninen reaktio, se reagoi heikommin antikolinergihoitoon. Neuroleptiparkinsonismille on ominaista spontaanin motorisen taidon heikkeneminen, hypo- ja amimia, lepovapina ja jäykkyys. On tärkeää erottaa nämä oireet skitsofrenian ulkoisesti samankaltaisista negatiivisista häiriöistä, joita edustavat emotionaalinen vieraantuminen, tunteiden lamaantuminen ja energian puute. Näiden sivuvaikutusten korjaamiseksi on aiheellista käyttää antikolinergisiä aineita, pienentää neuroleptin annosta tai korvata se epätyypillisellä antipsykoottisella lääkkeellä. Akatisia ilmenee sisäisenä ahdistuksena, kyvyttömyytenä pysyä yhdessä paikassa pitkään ja tarpeena jatkuvasti liikuttaa käsiä tai jalkoja. Sen lievittämiseksi käytetään antikolinergisiä aineita ja keskushermoston beetasalpaajia (propranololia).
Myöhäinen dyskinesia ilmenee minkä tahansa lihasryhmän, useimmiten kielen ja suun lihasten, tahattomina liikkeinä. Kliinisesti erotetaan useita sen muotoja: poskien, kielen ja suun lihasten dyskinesia (purentalihasten säännölliset supistukset, jotka luovat vaikutelman irvistävästä henkilöstä, kieli voi tahattomasti työntyä potilaan suusta); tardiivi dystonia ja tardiivi akatisia (potilas tekee koreoatetoidisia pään, vartalon, ylä- ja alaraajojen liikkeitä). Tätä häiriömuotoa havaitaan pääasiassa pitkäaikaisen perinteisten neuroleptien käytön aikana, ja sitä havaitaan noin 15–20 %:lla potilaista, jotka käyttävät niitä ylläpitohoitona. Todennäköisesti joillakin potilailla dyskinesian oireiden kehittymisen riski on lisääntynyt, koska joitakin niistä havaittiin skitsofrenian klinikalla jo ennen "neuroleptien aikakautta". Lisäksi tardiivia dyskinesiaa on kuvattu iäkkäillä naisilla ja mielialahäiriöistä kärsivillä potilailla. Tardiivin dyskinesian uskotaan liittyvän dopamiinireseptorien määrän lisääntymiseen striatumissa, vaikka GABAergiset ja muut välittäjäainejärjestelmät ovat todennäköisesti myös osallisina sen patogeneesissä. Näihin sivuvaikutuksiin ei ole tehokasta yleishoitoa. On ehdotettu, että pienillä annoksilla dopamiinia estäviä, tehokkaita neuroleptejä tai E-vitamiinia voi olla kohtalainen hyödyllinen vaikutus näihin häiriöihin. Tehokkain toimenpide tardiivin dyskinesian hoidossa on tyypillisen neuroleptin annoksen pienentäminen tai sen korvaaminen epätyypillisellä antipsykoottilla.
Nykyisten tietojen mukaan pahanlaatuista neuroleptioireyhtymää esiintyy noin 0,5 %:lla psykofarmakoterapian tapauksista. Todennäköisesti tällaisen hengenvaarallisen komplikaation harvinainen esiintyminen voidaan tällä hetkellä selittää epätyypillisten antipsykoottien laajamittaisella käyttöönotolla, koska malignin neuroleptioireyhtymän (MNS) kehittymisen riski näiden lääkkeiden käytön aikana on merkityksetön. Yleisesti hyväksytään, että MNS:n kehittymisen pääasiallinen syy on dopaminergisen järjestelmän liiallinen estyminen neuroleptihoidon aikana, erityisesti erittäin tehokkaan antipsykoottisen lääkkeen annoksen nostamisen jälkeen. MNS:n pääoireita ovat hypertermia, lisääntynyt luustolihasten ja jännerefleksien sävy, tajunnan heikkeneminen ja siirtyminen koomaan. Verikokeissa havaitaan leukosytoosia, lisääntynyttä punasolujen sedimentaatiota ja maksan transaminaasien aktiivisuutta; virtsakokeissa havaitaan albuminuriaa. Neste- ja elektrolyyttitasapainon häiriöt ilmenevät nopeasti, mikä luo edellytykset aivoödeeman muodostumiselle. MNS on akuutti tila, joka vaatii potilaan kiireellistä sairaalahoitoa intensiivistä infuusiohoitoa varten. MNS:n hoidossa tärkeintä on nesteytys ja oireenmukainen hoito. Tässä tilanteessa kaikki määrätyt neuroleptit on lopetettava välittömästi. Joissakin tapauksissa dopamiinireseptoriagonisteilla (esimerkiksi bromokriptiinillä) tai lihasrelaksanteilla on positiivinen vaikutus, vaikka niiden tehokkuutta ei ole tutkittu. Malignin neuroleptin poistamisen jälkeen neuroleptihoitoa ei tule aloittaa uudelleen vähintään kahteen viikkoon. Myöhemmin voidaan määrätä matalan tehon antipsykoottinen lääke, mieluiten uuden sukupolven lääke. Uuden lääkkeen annosta tulee lisätä erittäin huolellisesti, ja elintoimintojen tilaa ja laboratoriotuloksia (veri- ja virtsakokeet) tulee seurata.
Tyypilliset neuroleptit aiheuttavat harvoin vaarallisia ja kuolemaan johtavia komplikaatioita. Yliannostusoireet liittyvät pääasiassa lääkkeen antiadrenergisen ja antikolinergisen vaikutuksen yksilölliseen profiiliin. Koska näillä lääkkeillä on voimakas antiemeettinen vaikutus, niiden poistamiseksi elimistöstä on aiheellista tehdä mahahuuhtelu eikä antaa oksennuslääkkeitä. Valtimoiden hypotensio on yleensä seurausta adrenergisten reseptorien salpauksesta, ja se tulee korjata antamalla dopamiinia ja noradrenaliinia. Sydämen rytmihäiriöiden sattuessa on aiheellista käyttää lidokaiinia.
Tyypillisten antipsykoottien vaikutusmekanismi ja farmakologiset vaikutukset
Psykofarmakologian kehittyessä antipsykoottien vaikutuksesta neuroreseptoreihin on ehdotettu useita vaihtoehtoja. Päähypoteesi on edelleen, että ne vaikuttavat dopamiinin neurorakenteisiin (pääasiassa D2-reseptoreihin), mikä perustuu tietoihin normaalin dopamiiniaineenvaihdunnan häiriöistä aivorakenteissa psykooseissa. Dopamiini D2 -reseptorit sijaitsevat tyvitumakkeissa, nucleus accumbensissa ja otsalohkossa; niillä on johtava rooli tiedonkulun säätelyssä aivokuoren ja talamuksen välillä.
Kuva havainnollistaa yksityiskohtaisempaa ymmärrystä dopamiinin siirtymisen häiriöistä aivojen kortikaalisilla ja subkortikaalisilla alueilla sekä näiden häiriöiden roolista skitsofreniaoireiden kehittymisessä (mukailtu Jones RB:n monografiasta, Buckley PF, 2006).
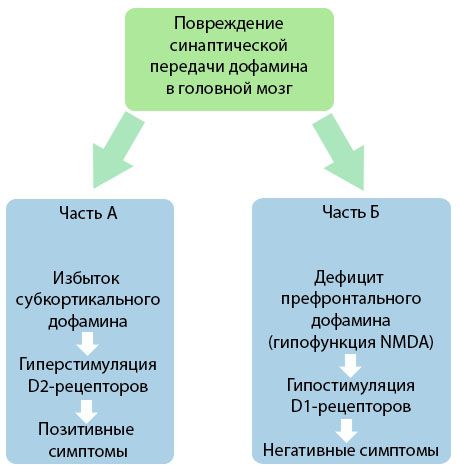
Osa A heijastaa klassista, varhaista dopamiiniteoriaa, joka olettaa dopamiinin liikatuotannon subkortikaalisilla alueilla ja D2-reseptorien hyperstimulaation, mikä johtaa tuotannollisten oireiden ilmaantumiseen. Osa B osoittaa teorian myöhemmän modernisoinnin 1990-luvun alussa. Tähän mennessä saadut tiedot paljastivat, että dopamiinin puutos D-reseptoreissa yhdessä näiden reseptorien riittämättömän stimulaation kanssa prefrontaalisessa aivokuoressa johtaa negatiivisten oireiden ja kognitiivisten häiriöiden ilmaantumiseen. Siksi nykykäsityksen mukaan molemmat dopaminergisen välittymisen häiriötyypit - subkortikaalinen dopamiinin liikatuotanto ja sen puutos prefrontaalisessa aivokuoressa - ovat yhteistulosta synaptisen välittymisen häiriöstä prefrontaalisella alueella ja liittyvät N-metyyli-N-aspartaatin vajaatoimintaan. Alun perin eristetyn dopamiinin lisäksi myöhemmin tunnistettiin muita skitsofrenian patogeneesiin osallistuvia välittäjäaineita, kuten serotoniini, gamma-aminovoihappo, glutamaatti, noradrenaliini, asetyylikoliini ja erilaiset neuropeptidit. Vaikka näiden välittäjäaineiden roolia ei ole täysin tutkittu, tiedon kehittyessä käy selväksi, että lukuisten neurokemiallisten muutosten ilmentyminen kehossa. Siksi antipsykoottisen lääkkeen kliininen vaikutus on yhteenveto vaikutuksista erilaisiin reseptorimuodostelmiin ja johtaa homeostaasihäiriöiden poistamiseen.
Viime vuosina uusien tutkimusmenetelmien, kuten radioisotooppiligandin sitoutumisen ja PET-kuvauksen, ansiosta on edistytty merkittävästi neuroleptien hienojen biokemiallisten vaikutusmekanismien selvittämisessä. Erityisesti on määritetty lääkkeiden suhteellinen voimakkuus ja tropismi sitoutua yksittäisiin neuroreseptoreihin aivojen eri alueilla ja rakenteissa. Lääkkeen antipsykoottisen vaikutuksen voimakkuuden on osoitettu riippuvan suoraan sen salpaavan vaikutuksen voimakkuudesta erilaisiin dopaminergisiin reseptoreihin. Viime aikoina on tunnistettu neljä tällaista reseptorityyppiä:
- D1 sijaitsevat pääasiassa mustatumakkeen ja striatumin alueella (ns. nigrostriataalinen alue) sekä prefrontaalisella alueella;
- D2 - nigrostriataalisissa, mesolimbisissa alueilla ja aivolisäkkeen etuosassa (prolaktiinin eritys);
- D3 (presynaptinen) - kontrolloi dopaminergistä aktiivisuutta negatiivisen palautteen lain mukaisesti eri aivorakenteissa;
- D4 (presynaptinen) - pääasiassa nigrostriataalisella ja mesolimbisellä alueella.
Samalla voidaan nyt pitää todistettuna, että juuri D2-reseptorien salpaus aiheuttaa antipsykoottisten, toissijaisten rauhoittavien vaikutusten sekä ekstrapyramidaalisten sivuvaikutusten kehittymistä. Muita tämän tyyppisten reseptorien salpauksen kliinisiä ilmentymiä ovat neuroleptien kipua lievittävä ja pahoinvointia lievittävä vaikutus (pahoinvoinnin ja oksentelun väheneminen oksennuskeskuksen lamautumisen seurauksena) sekä kasvuhormonin määrän väheneminen ja prolaktiinin tuotannon lisääntyminen (neuroendokriiniset sivuvaikutukset, mukaan lukien galaktorrea ja kuukautishäiriöt). Nigrostriaattisten D2-reseptorien pitkäaikainen salpaus johtaa niiden yliherkkyyden ilmenemiseen, joka on vastuussa tardiivin dyskinesian ja "yliherkkyyspsykoosien" kehittymisestä. Presynaptisten D3- ja D4-reseptorien salpauksen todennäköiset kliiniset ilmentymät liittyvät pääasiassa neuroleptien stimuloivaan vaikutukseen. Näiden nigrostriataalisen ja mesolimbokortikaalisen alueen reseptorien osittaisen salpauksen vuoksi aktivoivat ja inkisioivat (tehokkaat, erittäin aktiiviset) neuroleptit voivat pieninä annoksina stimuloida ja suurina annoksina estää dopamiinin siirtymistä.
Viime vuosina kiinnostus aivojen serotonergisten järjestelmien, mukaan lukien serotoniinireseptorien, toimintaan on lisääntynyt jyrkästi. Tosiasia on, että aivojen eri osissa serotonergisella järjestelmällä on moduloiva vaikutus dopaminergisiin rakenteisiin. Erityisesti mesokortikaalisella alueella serotoniini estää dopamiinin vapautumista, ja vastaavasti postsynaptisten 5-HT1A-reseptorien salpaus johtaa dopamiinipitoisuuden nousuun. Kuten tiedetään, skitsofrenian negatiivisten oireiden kehittyminen liittyy dopamiinineuronien vajaatoimintaan aivokuoren prefrontaalisissa rakenteissa. Tällä hetkellä tunnetaan noin 15 erilaista keskushermoston 5-HT1A-reseptoria. Kokeellisesti on havaittu, että neuroleptit sitoutuvat pääasiassa kolmen ensimmäisen tyypin 5-HT1A-reseptoreihin.
Näillä lääkkeillä on pääasiassa stimuloiva (agonistinen) vaikutus 5-HT1a-reseptoreihin. Todennäköiset kliiniset seuraukset: lisääntynyt antipsykoottinen vaikutus, kognitiivisten häiriöiden vaikeusasteen väheneminen, negatiivisten oireiden korjaantuminen, masennuslääkevaikutus ja ekstrapyramidaalisten sivuvaikutusten esiintyvyyden väheneminen.
Neuroleptien vaikutus 5-HT2-reseptoreihin, erityisesti 5-HT2a-alatyyppeihin, on merkittävä. Ne sijaitsevat pääasiassa aivokuoressa ja niiden herkkyys on lisääntynyt skitsofreniapotilailla. Uuden sukupolven neuroleptien kyky vähentää negatiivisten oireiden vakavuutta, parantaa kognitiivisia toimintoja, säädellä unta pidentämällä hitaan aallon (D-aallon) unen vaiheiden kokonaiskestoa, vähentää aggressiivisuutta ja lievittää masennusoireita ja migreenin kaltaisia (aivoverisuonihäiriöistä johtuvia) päänsärkyjä liittyy 5-HT2a-reseptorien salpaukseen. Toisaalta 5-HT2a-reseptorien salpaus voi aiheuttaa miehillä verenpainetta alentavia vaikutuksia ja siemensyöksyhäiriöitä.
Neuroleptien vaikutuksen 5-HT2c-reseptoreihin uskotaan aiheuttavan rauhoittavan (anksiolyyttisen) vaikutuksen, lisääntyneen ruokahalun (johon liittyy painonnousu) ja prolaktiinin tuotannon vähenemisen.
5-HT3-reseptorit sijaitsevat pääasiassa limbisessä hermostossa, ja kun ne estyvät, pahoinvointia estävä vaikutus kehittyy ensin, ja myös antipsykoottiset ja anksiolyyttiset vaikutukset voimistuvat.
Parkinsonin taudin kaltaisten oireiden esiintyminen riippuu myös lääkkeen muskariinikolinergisiin reseptoreihin kohdistuvasta salpausvoimasta. Kolinolyyttiset ja dopamiinia estävät vaikutukset ovat jossain määrin vastavuoroisessa suhteessa toisiinsa. Tiedetään esimerkiksi, että nigrostriataalialueella D2-reseptorit estävät asetyylikoliinin vapautumista. Kun yli 75 % nigrostriataalialueen D2-reseptoreista on estetty, tasapaino häiriintyy kolinergisen järjestelmän hyväksi. Tämä on syynä antikolinergisten lääkkeiden (korjaajien) korjaavaan vaikutukseen neuroleptien ekstrapyramidaalisiin sivuvaikutuksiin. Klooriprotikseenilla, klotsapiinilla ja olantsapiinilla on suuri affiniteetti muskariinireseptoreihin, eivätkä ne käytännössä aiheuta ekstrapyramidaalisia sivuvaikutuksia, koska ne salpaavat kolinergisiä ja dopaminergisiä reseptoreita samanaikaisesti. Haloperidoli- ja piperatsiinifenotiatsiinijohdannaisilla on voimakas vaikutus dopamiinireseptoreihin, mutta hyvin heikko vaikutus koliinireseptoreihin. Tämä johtuu niiden kyvystä aiheuttaa voimakkaita ekstrapyramidaalisia sivuvaikutuksia, jotka vähenevät käytettäessä erittäin suuria annoksia, kun kolinolyyttinen vaikutus tulee havaittavaksi. Sen lisäksi, että voimakas kolinerginen vaikutus vähentää dopamiinia estävää vaikutusta nigrostriataalisen alueen D2-reseptoreihin ja tasoittaa ekstrapyramidaalisia sivuvaikutuksia, se voi aiheuttaa kognitiivisten toimintojen heikkenemistä, mukaan lukien muistihäiriöitä, sekä perifeerisiä sivuvaikutuksia (kuivat limakalvot, heikentynyt näköaisti, ummetus, virtsaumpi, sekavuus jne.). Neurolepteillä on melko voimakas estävä vaikutus tyypin I histamiinireseptoreihin, mikä liittyy ensinnäkin rauhoittavan vaikutuksen voimakkuuteen sekä lisääntyneestä ruokahalusta johtuvaan painonnousuun. Neuroleptien antiallergiset ja kutinaa estävät vaikutukset liittyvät myös niiden antihistamiiniominaisuuksiin.
Dopamiinia salpaavien, antiserotonergisten, kolinolyyttisten ja antihistamiinivaikutusten lisäksi useimmilla neurolepteillä on adrenolyyttisiä ominaisuuksia eli ne salpaavat sekä keskushermoston että perifeerisiä a1-adrenoreseptoreita. Adrenoblokkereilla, kuten klooripromatsiinilla ja klooriprotikseenillä, on voimakas sedatiivinen vaikutus. Lisäksi näiden lääkkeiden salpaava vaikutus voi aiheuttaa neurovegetatiivisia sivuvaikutuksia (valtimon hypotensiota, takykardiaa jne.) sekä lisätä adrenoblokkereiden verenpainetta alentavaa vaikutusta.
Lukuisten kirjoittajien teokset tarjoavat tietoa yksittäisten neuroleptien sitoutumisvoimasta (affiniteetista) erityyppisiin neuroreseptoreihin.
Neurokemiallisen vaikutusprofiilinsa perusteella kliinisessä käytännössä pääasiassa käytetyistä tyypillisistä ja epätyypillisistä antipsykooteista voidaan ehdollisesti jakaa kuuteen ryhmään.
Ensimmäinen ryhmä koostuu selektiivisistä D2- ja D4-reseptorien salpaajista (sulpiridi, amisudpridi, haloperidoli jne.) bentsamidi- ja butyrofenonijohdannaisten ryhmistä. Pieninä annoksina, pääasiassa presynaptisten D4-reseptorien salpauksen vuoksi, ne aktivoivat hermoimpulssien dopaminergistä siirtymistä ja niillä on stimuloiva (estävä) vaikutus, suurina annoksina ne salpaavat D2-reseptoreita kaikilla aivojen alueilla, mikä ilmenee kliinisesti voimakkaana antipsykoottisena vaikutuksena sekä ekstrapyramidaalisina ja endokriinisinä (prolaktinemian vuoksi) sivuvaikutuksina.
Toiseen ryhmään kuuluvat erittäin aktiiviset D2-reseptorien salpaajat sekä lääkkeet, jotka salpaavat heikosti tai kohtalaisesti 5-HT2a- ja 5-HT1a-reseptoreita (flupentiksoli, flufenatsiini, tsuklopentiksoli jne.), eli pääasiassa fenotiatsiinin piperatsiinijohdannaisia tai niitä stereokemiallisessa rakenteessa lähellä olevia tioksanteeneja. Kuten ensimmäisen ryhmän lääkkeillä, näillä neurolepteillä on ensinnäkin voimakas antipsykoottinen (inkisiivinen) vaikutus, ja ne aiheuttavat myös ekstrapyramidaalisia närästysoireita ja prolaktinemiaa. Pieninä annoksina niillä on kohtalaisen aktivoiva (psykostimuloiva) vaikutus.
Kolmas ryhmä koostuu polyvalenteista sedatiivisista neurolepteistä, jotka salpaavat useimmat neuroreseptorit erilaistumattomalla tavalla. Näillä lääkkeillä on selvästi ilmentynyt dopamiinireseptoreiden salpausvaikutus, ja ne aiheuttavat myös voimakkaita adrenolyyttisiä ja kolinolyyttisiä vaikutuksia. Tähän kuuluvat useimmat sedatiiviset neuroleptit, pääasiassa fenotiatsiinin alifaattiset ja piperidiinijohdannaiset sekä niitä stereokemiallisessa rakenteessa lähellä olevat tioksanteenit (klooripromatsiini, levomepromatsiini, klooriprotikseeni jne.). Näiden lääkkeiden psykotrooppisen aktiivisuuden kirjoa hallitsee ensinnäkin voimakas primaarinen sedatiivinen vaikutus, joka kehittyy käytetystä annoksesta riippumatta, ja kohtalainen antipsykoottinen vaikutus. Lisäksi voimakkaan antikolinergisen vaikutuksensa vuoksi tämän ryhmän lääkkeet aiheuttavat heikkoja tai kohtalaisia ekstrapyramidaalisia ja neuroendokriinisiä sivuvaikutuksia, mutta usein ne johtavat ortostaattisen hypotension ja muiden autonomisten reaktioiden kehittymiseen johtuen voimakkaasta a1-adrenergisten reseptorien salpauksesta.
Neljänteen ryhmään kuuluvat neuroleptit, jotka salpaavat D2- ja 5-HT2a-reseptoreita tasapainoisesti eli samassa määrin (jälkimmäistä hieman suuremmassa määrin) ja kohtalaisessa määrin a1-adrenoreseptoreita. Tähän ryhmään kuuluvat uuden sukupolven epätyypillisten antipsykoottien (risperidoni, tsiprasidoni, sertindoli) edustajat, joilla on erilaiset kemialliset rakenteet. Neurokemiallinen vaikutusmekanismi määrää niiden selektiivisen vaikutuksen ensisijaisesti aivojen mesolimbisiin ja mesokortikaalisiin alueisiin. Selkeän antipsykoottisen vaikutuksen, ekstrapyramidaalisten sivuvaikutusten puuttumisen tai heikon ilmentymisen (terapeuttisia annoksia käytettäessä), heikon tai kohtalaisen prolaktinemian ja kohtalaisten adrenolyyttisten ominaisuuksien (hypotensiiviset reaktiot) ohella tämä neuroleptiryhmä pystyy korjaamaan negatiivisia oireita stimuloimalla epäsuorasti dopaminergistä signalointia aivokuoressa.
Viides ryhmä koostuu trisyklisen dibentsodiatsepiinin tai vastaavan rakenteen omaavista polyvalenteista epätyypillisistä antipsykooteista (klotsapiinista, olantsapiinista ja ketiapiinista). Aivan kuten kolmannen ryhmän lääkkeet, ne salpaavat useimpia neuroreseptoreita erilaistumattomalla tavalla. 5-HT2a-reseptorit salpautuvat kuitenkin voimakkaammin kuin D2- ja D4-reseptorit, erityisesti nigrostriataalialueella sijaitsevat reseptorit. Tämä määrää ekstrapyramidaalisen vaikutuksen tosiasiallisen puuttumisen tai heikon vaikutuksen sekä lisääntyneeseen prolaktiinituotantoon liittyvien neuroendokriinisten sivuvaikutusten puuttumisen, joilla on selkeä antipsykoottinen vaikutus ja kyky vähentää negatiivisten oireiden vakavuutta. Lisäksi kaikilla tämän ryhmän lääkkeillä on voimakkaita adrenolyyttisiä ja antihistamiinisia ominaisuuksia, jotka määräävät sedatiiviset ja verenpainetta alentavat vaikutukset. Klotsapiinilla ja olantsapiinilla on myös melko voimakas muskariinireseptoreiden salpausvaikutus, ja ne johtavat kolinolyyttisten sivuvaikutusten kehittymiseen.
Siten kyky estää postsynaptisia dopaminergisiä reseptoreita dopamiinin synteesin ja metabolian kompensoivalla lisääntymisellä on ainoa yhteinen biokemiallinen ominaisuus kaikille näissä ryhmissä tarkastelluille neurolepteille.
Kuudenteen ryhmään kuuluu ainoa epätyypillinen antipsykoottinen lääke, aripipratsoli, joka on ilmestynyt kotimaisille psykofarmakologisille markkinoille suhteellisen äskettäin. Tämä lääke on D2-dopamiinireseptorien osittainen agonisti ja toimii funktionaalisena antagonistina hyperdopaminergisessä tilassa ja funktionaalisena agonistina hypodopaminergisessä profiilissa. Aripipratsolin tällainen ainutlaatuinen reseptoriprofiili mahdollistaa ekstrapyramidaalisten häiriöiden ja hyperprolaktinemian riskin vähentämisen sitä käytettäessä. Lisäksi aripipratsoli toimii 5-HT1a-reseptorien osittaisena agonistina ja samalla se on 5-HT2a-reseptorien antagonisti. Oletetaan, että tällainen vuorovaikutus reseptorien kanssa johtaa serotoniini- ja dopamiinijärjestelmien yleisesti tasapainoiseen toimintaan, joten aripipratsolin vaikutusmekanismiksi voidaan kutsua dopamiini-serotoniinijärjestelmän stabilointia.
Näin ollen neuroleptien neurokemiallisten vaikutusmekanismien nykyinen tietämystaso antaa meille mahdollisuuden ehdottaa uutta, patogeneettisesti perustellumpaa farmakodynaamista luokittelua tälle psykotrooppisten lääkkeiden ryhmälle. Tämän luokituksen avulla voimme ennustaa pitkälti tietyn lääkkeen psykotrooppisen aktiivisuuden kirjon, toleranssin ja todennäköiset lääkeyhteisvaikutukset. Toisin sanoen lääkkeen neurokemiallisen aktiivisuuden ominaisuudet määräävät suurelta osin sen kliinisen aktiivisuuden ominaisuudet, joita tulisi käyttää valittaessa tiettyä antipsykoottista lääkettä tietylle potilaalle.
Minkä tahansa neuroleptin globaalin antipsykoottisen vaikutuksen tehokkuutta arvioidaan käyttämällä ns. klooripromatsiiniekvivalenttia, joka otetaan arvoksi 1. Esimerkiksi haloperidolin klooripromatsiiniekvivalentti on = 50. Tämä tarkoittaa, että 1 mg:n haloperidolin antipsykoottinen teho on verrattavissa 50 mg:aan klooripromatsiinia. Tämän indikaattorin perusteella on kehitetty luokittelu, joka mahdollistaa neuroleptien jakamisen, joilla on korkea (klooripromatsiiniekvivalentti > 10,0), keskitaso (klooripromatsiiniekvivalentti = 1,0-10,0) ja matala (klooripromatsiiniekvivalentti = 1,0) antipsykoottinen aktiivisuus, jota kutsutaan patentiteetiksi. Tyypillisiä neuroleptejä (ensimmäisen sukupolven antipsykootteja) on käytetty laajalti kliinisessä psykofarmakoterapiassa lähes puoli vuosisataa. Niiden terapeuttisen aktiivisuuden kirjo sisältää:
- globaali antipsykoottinen vaikutus kyvyn muodossa vähentää tasaisesti ja eri tavoin psykoosin eri ilmenemismuotoja:
- ensisijainen rauhoittava (estävä) vaikutus - lääkkeiden kyky lievittää nopeasti psykomotorista levottomuutta;
- valikoiva, selektiivinen antipsykoottinen vaikutus, joka ilmenee kyvyssä vaikuttaa yksittäisiin oireisiin: delirium, hallusinaatiot, käytöksen esto jne.;
- aktivoiva (estävä, estävä, antiautistinen) neurotrooppinen vaikutus, joka ilmenee ekstrapyramidaalisten oireiden kehittymisenä;
- somatotrooppinen vaikutus neuroendokriinisten ja vegetatiivisten sivuvaikutusten kehittymisen muodossa;
- lamauttava vaikutus, joka ilmenee joidenkin antipsykoottien kyvynä aiheuttaa masennusoireita.
Ensimmäisen sukupolven antipsykoottien tehokkuus paitsi psykoottisten häiriöiden, myös raja-arvopsykiatrian häiriöiden hoidossa on todistettu useita kertoja ja se on kiistaton. Siksi, huolimatta hoidon sivuvaikutusten suuresta esiintyvyydestä niitä määrättäessä, niitä käytetään edelleen lääketieteellisessä käytännössä.
Antipsykoottisen hoidon sivuvaikutukset
Taulukossa luetellaan epätyypillisen antipsykoottisen hoidon tärkeimmät sivuvaikutukset.
Valmistelu |
Ekstrapyramidaaliset |
Johtumishäiriö EKG:ssä |
Aineenvaihduntahäiriöt (painonnousu, kohonneet verensokeri-, kolesteroli- ja triglyseridipitoisuudet) |
||
Klotsapiini |
. |
++ |
++ |
++- |
|
Risperidoni |
++ |
+/- |
++ |
+/- |
|
Olantsapiini |
+ |
+/- |
+++ |
++ |
+++ |
Ketiapiini |
+/- |
+ |
+/- |
--- |
|
Tsiprasidoni |
+ |
++ |
+/- |
+/- |
+/- |
Sertindoli |
++ |
-- |
+/- |
-- |
|
Arilipratsoli |
-- |
--- |
+/- |
-- |
-- |
Amisulpridi |
++ |
+/- |
|||
Huomautus. Sivuvaikutusten vakavuus: "+++" - korkea; "++" - keskitaso; "+" - matala; "+/-" - kyseenalainen; "-" - puuttuu.
Ekstrapyramidaaliset oireyhtymät
Yksi epätyypillisten antipsykoottien pääpiirteistä perinteisiin verrattuna on niiden heikko kyky aiheuttaa ekstrapyramidaalisia oireyhtymiä, mikä oli läpimurto skitsofrenian ylläpitolääkehoidossa. Taulukon tiedoista kuitenkin käy ilmi, että yksittäisiä tämän sarjan lääkkeitä (risperidoni, amisulpridi) käytettäessä voi esiintyä tällaisia oireita, jotka vaativat erityistä huomiota niitä määrättäessä.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
EKG-poikkeavuudet
Sydänsivuvaikutusten mahdollisuus on vakava ongelma käytettäessä joitakin nykyaikaisia antipsykootteja terapiassa. Näissä tapauksissa puhumme QT-ajan pidentymisestä, joka voi johtaa rytmihäiriöiden kehittymiseen. Johtumishäiriöitä, ensisijaisesti QT-ajan pidentymistä, havaitaan useimmiten klotsapiini-, sertindol- ja tsiprasidonihoidon aikana. Samanaikainen sairaus, kuten bradykardia, eteis-kammiokatkos ja kilpirauhasen vajaatoiminta, voi edistää tämän komplikaation esiintymistä edellä mainittujen lääkkeiden käytön aikana. Tällä hetkellä EKG-seurantaa suositellaan noin kerran kolmessa kuukaudessa potilaille, jotka saavat ylläpitohoitoa epätyypillisillä antipsykooteilla.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Umpierityshäiriöt
Tällä hetkellä suurinta huolta aiheuttaa epätyypillisten antipsykoottisten lääkkeiden kyky aiheuttaa painonnousua. Kohonnut paino, verensokeri- ja triglyseriditasot voivat johtaa aineenvaihduntahäiriöihin ja tyypin 2 diabeteksen kehittymiseen. Erityistä varovaisuutta ja biokemiallisten parametrien viikoittaista seurantaa tarvitaan klotsapiini- ja olantsapiinihoidon aikana. J. Geddesin ym. (2000), PB Jonesin ja PF Buckleyn (2006) mukaan on pidettävä tarkoituksenmukaisena suorittaa perusteellinen potilastutkimus ennen tietyn nykyaikaisen sukupolven antipsykootin määräämistä, koska tiedetään, että aineenvaihduntahäiriöitä esiintyy useammin potilailla, joilla oli perinnöllinen alttius, ylipaino, lipidispektrin häiriöt ja hyperglykemia ennen hoidon aloittamista. PB Jonesin ja PF Buckleyn (2006) ehdottama seuranta-algoritmi sisältää useita kohtia.
- Sairaushistorian ja perhetekijöiden kerääminen aineenvaihduntahäiriöiden riskiin liittyen.
- Painoindeksin, EKG:n, verenpaineen ja pulssin rekisteröinti ennen hoidon aloittamista.
- Laboratoriotietojen (glukoosi, lipidiprofiili, kolesteroli) kerääminen ennen hoidon aloittamista.
- Painoindeksin ja elintoimintojen säännöllinen seuranta hoidon aikana.
- Laboratoriotietojen seuranta hoidon aikana.
Hyperprolaktinemian esiintyminen antipsykoottisen hoidon aikana johtuu hypotalamuksen dopamiinireseptorien keskushermoston salpauksesta, mikä johtaa prolaktiinin vapautumiseen aivolisäkkeen etulohkosta. Hyperprolaktinemiaa esiintyy useimmiten olantsapiini-, risperidoni- ja amisulpridihoidon yhteydessä.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Agranulosytoosi
Toinen vakava antipsykoottisen hoidon komplikaatio. Se voidaan havaita klotsapiini- ja olantsapiinihoidon aikana. J. Geddesin ym. (2000) mukaan se diagnosoitiin ensimmäisten 3 kuukauden aikana 1–2 %:lla näitä lääkkeitä käyttävistä potilaista. Tässä suhteessa suositellaan viikoittaisia verikokeita potilaille, jotka käyttävät näitä lääkkeitä ensimmäisten 18 hoitoviikon aikana, ja sen jälkeen kuukausittaista seurantaa. On osoitettu, että kun edellä mainittujen neuroleptien annosta pienennetään, kliininen verikoe palautuu normaaliksi. Samalla on tunnustettava, että tähän mennessä ei ole olemassa selkeää strategiaa potilaille, joilla ilmenee edellä mainittuja aineenvaihduntahäiriöihin liittyviä sivuvaikutuksia. Useimmiten yksi epätyypillinen antipsykootti korvataan toisella. Toinen lupaava suunta on erityisen korjaavan hoidon määrääminen, erityisesti bromokriptiinin käyttö hyperprolaktinemian korjaamiseksi. Ihanteellinen tilanne on sellainen, jossa tällaisista sairauksista kärsivän potilaan hoito suoritetaan sisätautien lääkäreiden, erityisesti endokrinologien, kardiologien ja muiden asiantuntijoiden, säännöllisessä osallistumisessa.
Yhteenvetona on todettava, että jos noudatetaan annettuja algoritmeja potilaiden henkisen ja fyysisen tilan määräämiseen ja seurantaan, toisen sukupolven lääkkeiden käyttö on turvallisempaa kuin tyypillisten neuroleptien.
Useita muita antipsykootteja on parhaillaan kehitysvaiheessa. Seuraavan sukupolven lääkkeillä on todennäköisesti erilainen vaikutusmekanismi (esimerkiksi GABAerginen profiili) ja ne pystyvät vaikuttamaan skitsofrenian erilaisiin ilmentymiin, mukaan lukien varsinaiset alijäämähäiriöt.
Epätyypilliset antipsykootit
Nykyaikaiset ohjeet sisältävät tietoa toisen sukupolven antipsykoottien käytön eduista lääkehoidossa. Termi "epätyypillinen" (synonyymi - toisen sukupolven antipsykootit) on ehdollinen ja sitä käytetään pääasiassa uuden sukupolven nimeämisen helpottamiseksi. Verrattuna perinteisiin neurolepteihin, tämän ryhmän lääkkeet ovat tehokkaampia negatiivisten, affektiivisten ja kognitiivisten häiriöiden korjaamisessa, mikä yhdistyy parempaan siedettävyyteen ja pienempään ekstrapyramidaalisten oireiden riskiin. Yhden tai toisen lääkkeen terapeuttisen vaikutuksen luonteen erot useista epätyypillisistä antipsykooteista selittyvät, kuten tyypillisten neuroleptien ryhmässä, sen yksilöllisellä farmakologisen vaikutuksen profiililla.
Psykofarmakoterapian mahdollisuuksien selventämiseksi epätyypillisillä antipsykooteilla on suositeltavaa keskittyä tämän ryhmän lääkkeisiin, jotka on rekisteröity Venäjällä.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Klotsapiini (dibentsodiatsepiini)
Epätyypillisten antipsykoottien ryhmän perustaja. Klotsapiinin vaikutusmekanismille on ominaista D2-reseptorien lievä salpaus ja samanaikainen voimakas antagonismi 5-HT2a-reseptoreita, a1-, a2-adrenergisiä ja H1-histamiinireseptoreita kohtaan. Se on osoittautunut tehokkaaksi antipsykoottiseksi lääkkeeksi resistenssin tapauksissa muille antipsykooteille (reserviryhmän lääke), ja sitä käytetään myös kroonisen manian, psykoottisen agitaation ja aggressiivisuuden hoitoon. Kotimaisessa käytännössä klotsapiinia määrätään usein sedaation saavuttamiseksi ja hypnoottisena lääkkeenä psykoottisille potilaille. On ymmärrettävä, että klotsapiinin tällainen käyttö ei vastaa sen pääasiallista terapeuttista käyttöaihetta. Todennäköisesti suhtautumista tähän antipsykoottiseen lääkkeeseen toissijaisena lääkkeenä tulisi tarkistaa, koska nykyään se on ainoa lääke, jolla on todistettu teho resistenteillä potilailla.
Toisin kuin tyypilliset neuroleptit, klotsapiini ei aiheuta vakavia ekstrapyramidaalisia häiriöitä edellä mainitun alhaisen O2-reseptoriaffiniteetin vuoksi. Osoittautui myös, että sitä voidaan käyttää myöhäisen dystonian ja vaikean akatisian hoitoon. Koska malignin neuroleptioireyhtymän (NMS) kehittymisriski on alhainen, klotsapiinia voidaan pitää ensisijaisena lääkkeenä potilaille, jotka ovat aiemmin kärsineet tästä komplikaatiosta.
Klotsapiinihoidon aikana voi kuitenkin kehittyä useita vakavia sivuvaikutuksia. Vaarallisin niistä (jopa pienillä annoksilla) on agranulosytoosi, jota esiintyy 0,5–1,0 %:lla potilaista. Muita tärkeitä sivuvaikutuksia, joita voi esiintyä lääkkeen käytön aikana, ovat uneliaisuus, lisääntynyt syljeneritys ja painonnousu, joka on usein jo kohonnut klotsapiinin määräyshetkellä aiemman antipsykoottisen hoidon vaikutuksesta. Huomiota on kiinnitettävä myös takykardian, valtimoiden hypotension ja epileptisten kohtausten mahdollisuuteen lääkkeen käytön aikana. Kouristusten todennäköisyys riippuu annoksesta. Niiden riski kasvaa merkittävästi, jos klotsapiiniannos ylittää 600 mg/vrk. Kouristusten kehittyminen ei ole vasta-aihe lääkkeen jatkokäytölle, mutta se vaatii annoksen puolittamista ja antikonvulsiivisten lääkkeiden, kuten valproiinihapon, määräämistä. Klotsapiinihoidon sivuvaikutusten ehkäisyyn kuuluu valkosolujen määrän sekä EKG:n ja endokriinisten parametrien huolellinen seuranta.
Klotsapiinin yliannostus voi aiheuttaa tajunnantason laskua jopa koomaan asti, sekä kolinolyyttiseen vaikutukseen liittyviä oireita (takykardia, delirium), epileptisiä kohtauksia, hengityslamaa ja ekstrapyramidaalisia oireyhtymiä. Yli 2500 mg:n annos voi johtaa kuolemaan.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Risperidoni
Bentsisoksatsolijohdannainen, jolla on korkea affiniteetti serotoniini- ja dopamiini-Dj-reseptoreihin ja pääasiallinen vaikutus serotoniinijärjestelmään. Lääkkeellä on laaja valikoima käyttöaiheita, mukaan lukien pahenemisvaiheiden lievitys, uusiutumisen estohoito, ensimmäisen psykoottisen jakson hoito ja skitsofrenian negatiivisten oireiden korjaus. Lääkkeen on osoitettu parantavan kognitiivisia toimintoja skitsofreniapotilailla. Alustavien tietojen mukaan risperidoni vähentää myös samanaikaisia affektiivisia oireita skitsofreniapotilailla ja voi olla ensisijainen lääke kaksisuuntaisen mielialahäiriön hoidossa.
Risperidonihoidon sivuvaikutukset, erityisesti ekstrapyramidaaliset häiriöt, ovat annoksesta riippuvaisia ja esiintyvät useammin yli 6 mg/vrk annoksilla. Muita sivuvaikutuksia ovat pahoinvointi, oksentelu, ahdistuneisuus, uneliaisuus ja kohonneet seerumin prolaktiinipitoisuudet. Risperidonin pitkäaikainen käyttö voi johtaa painonnousuun ja tyypin 2 diabeteksen kehittymiseen, mutta pienemmällä todennäköisyydellä kuin klotsapiinilla tai olantsapiinilla.
Yliannostus voi aiheuttaa uneliaisuutta, epileptisiä kohtauksia, QT-ajan pidentymistä ja QRS-kompleksin laajenemista sekä valtimoiden hypotensiota. Risperidonin yliannostuksesta on kuvattu kuolemaan johtaneita tapauksia.
Lääkkeen kiistaton etu on nestemäisten ja nopeasti liukenevien (kielenalaisesti annosteltavien) muotojen saatavuus, joiden käyttö nopeuttaa lääkkeen imeytymistä potilaan elimistöön ja helpottaa sen saannin hallintaa. Lääkkeestä on myös pitkäaikainen muoto - jauhe lihaksensisäisen suspension valmistamiseksi (consta-risperidoni mikropalloina). Sitä suositellaan skitsofreniapotilaiden ylläpitohoitoon, erityisesti potilaille, joilla on huono hoitomyöntyvyyde. On otettava huomioon, että lääkkeen imeytyminen verenkiertoon kestää noin kolme viikkoa, joten consta-risperidonihoitoa aloitettaessa potilaan on otettava lisäksi risperidonia suun kautta vähintään 3 viikon ajan ensimmäisen injektion jälkeen.
Olantsapiini
Farmakologisen vaikutuksen suhteen se on lähellä klotsapiinia, koska sillä on pleiomorfinen reseptoriprofiili, jolla on merkittävä affiniteetti serotoniini-, muskariini-, α1-adrenergisiin ja histamiinireseptoreihin. Olantsapiinin terapeuttinen aktiivisuus on samanlaista kuin klotsapiinin ja risperidonin tehokkuuden skitsofrenian positiivisiin, negatiivisiin ja masennusoireisiin kohdistuvan vaikutuksen suhteen. Samalla on saatu tietoa olantsapiinin suuremmasta tehokkuudesta verrattuna muihin epätyypillisiin antipsykoottisiin lääkkeisiin potilailla, joilla on ensimmäinen psykoottinen episodi, ja kognitiivisten toimintakyvyn indikaattoreiden korjauksessa. On otettava huomioon, että hoidon alussa lääkkeen tablettimuotoa käytettäessä voi ilmetä nopea disinhibitorinen vaikutus, johon liittyy lisääntynyttä psykomotorista agitaatiota ja ahdistusta. Siksi vaikeaan psykomotoriseen agitaatioon liittyvien kohtausten hoidossa lääkkeen injektiomuoto on aiheellista käyttää.
Olantsapiini aiheuttaa harvoin ekstrapyramidaalisia häiriöitä tai tardiivia dyskinesiaa, ja yleisimmät sen käytön sivuvaikutukset ovat aineenvaihduntahäiriöt ja painonnousu. On todettu, että olantsapiinia saavilla potilailla esiintyy melko usein kohonneita kolesteroli- ja plasman lipidiarvoja sekä alttiutta tyypin 2 diabetekselle, mutta tällaiset vaikutukset olivat yhtä yleisiä sekä olantsapiinia että klotsapiinia saaneilla potilailla. Samalla on saatu tietoja, jotka osoittavat, että painonnousu korreloi positiivisen olantsapiinivasteen kanssa (eli toimii tärkeänä hoitoennusteena) ja kehittyy lihavuudeksi vain 20–30 %:lla potilaista, jotka ovat lihonneet hoidon aikana.
Yliannostus voi aiheuttaa sedaatiota, toksisia antikolinergisiä vaikutuksia, epileptisiä kohtauksia ja valtimoiden hypotensiota. Tällä hetkellä ei ole vakuuttavia tietoja yliannostuksen aiheuttaman kuoleman riskin arvioimiseksi.
Ketiapiini
Se luokitellaan dibentsotiatsepiiniyhdisteeksi. Sen reseptoriprofiili on pitkälti samanlainen kuin klotsapiinilla. Ketiapiinin sitoutumisaste D2-reseptoreihin on alhainen (alle 50 %) ja lyhytaikainen jopa suurina annoksina. Lääke on tehokas skitsofrenian positiivisten, negatiivisten ja yleisten oireiden hoidossa. Sen onnistuneesta käytöstä on näyttöä sekä korkean hoitoresistenssin tapauksissa että potilaiden kognitiivisten toimintakyvyn parantamisessa, mikä antaa oikeuden suositella sitä ensisijaiseksi antipsykootiksi skitsofrenian ylläpitohoitoon. Lopuksi, ketiapiinilla on kohtalainen masennuslääke, aktivoiva vaikutus. Siksi sitä käytetään masennus-harhakohtausten ja senesto-hypokondriaalisen aivojen piirin häiriöiden hoitoon.
Ketiapiinin todettu korkea tymotrooppinen aktiivisuus selittää sen, miksi se on rekisteröity masennushäiriöiden lievitykseen ja toissijaiseen ehkäisyyn. Kaksisuuntaisen mielialahäiriön tyypin I ja II maanisten jaksojen hoidossa ketiapiinia käytetään lisäkeinona. Injektiomuotojen puuttuminen rajoittaa jonkin verran sen käyttöä potilailla, joilla on agitaatiota ja aggressiivista käyttäytymistä.
Ketiapiini on hyvin siedetty, se ei käytännössä aiheuta ekstrapyramidaalisia oireyhtymiä, paitsi tapauksissa, joissa käytetään maksimiannoksia. Ketiapiini ei aiheuta hyperprolaktinemiaa, harvemmin kuin olantsapiini ja klotsapiini, se johtaa painonnousuun ja heikentyneeseen glukoosinsietoon.
Tsiprasidoni
Sillä on ainutlaatuinen reseptoriaktiivisuusprofiili. Koska se on voimakas 5HT2a- ja D2-reseptorien antagonisti, se on myös aktiivinen serotoniinin ja noradrenaliinin takaisinoton estäjä. Kliiniset tutkimukset ovat osoittaneet tsiprasidonin merkittävän paremman vaikutuksen psykoottisiin oireisiin ja aggressiivisuuden ilmenemismuotoihin verrattuna haloperidoliin. On myös tietoa tsiprasidonin positiivisesta vaikutuksesta skitsofreniaa sairastavien potilaiden kognitiivisiin toimintoihin sekä samanaikaisiin affektiivisiin oireisiin ja sosiaalisen toimintakyvyn indikaattoreihin. Tsiprasidoni on yleensä hyvin siedetty ja aiheuttaa hyvin harvoin ekstrapyramidaalisia oireyhtymiä, painonnousua ja aineenvaihduntahäiriöitä. Useammin QT-aika pidentyy yli 460 ms:iin, joten tätä lääkettä saaville potilaille on suositeltavaa tehdä EKG-tutkimus sekä ennen lääkkeen määräämistä että kontrolloidusti hoidon aikana. Erityistä huomiota on kiinnitettävä samanaikaiseen hoitoon (rytmihäiriölääkkeiden käyttö), joka voi pahentaa QT-ajan pidentymistä ja johtaa sydämen rytmihäiriöiden ja kammiovärinän kehittymiseen.
Sertindoli
Kuuluu fenyyliindolin johdannaisiin. Sillä on voimakas toiminnallinen antagonismi D2-, serotoniini- (erityisesti 5-HT2a-reseptoreihin) ja a1-adrenergisiin reseptoreihin. Elektroneurokemiallisten tutkimusten mukaan sertindoli estää selektiivisesti dopamiinireseptoreita vatsalohkon segmenttialueella. Tällainen selektiivisyys todennäköisesti varmistaa ekstrapyramidaalisten oireyhtymien ja hyperprolaktinemian pienen riskin lääkettä käytettäessä. Vertailevien tutkimusten tulokset ovat osoittaneet, että sertindolin antipsykoottinen aktiivisuus on verrattavissa haloperidoliin. Lääkkeellä on voimakas disinhibitorinen vaikutus negatiivisia ja masennusoireita sairastavilla potilailla, mikä on parempi kuin rispoleptin vastaava vaikutus. On myös näyttöä sertindolin tehokkuudesta skitsofreniapotilaiden kognitiivisten häiriöiden korjaamisessa. Potilaat sietävät sertindolia yleensä hyvin, se aiheuttaa harvoin sedaatiota ja siksi sitä suositellaan korvaavaksi lääkkeeksi, kun muita nykyaikaisia antipsykootteja käytettäessä ilmenee sivuvaikutuksia.
Vakaviin sivuvaikutuksiin kuuluu lääkkeen kyky pidentää QT-aikaa, mikä voi johtaa sydämen rytmihäiriöihin. Markkinoille tulon jälkeisiä tutkimuksia analysoitaessa kävi selväksi, että sertindolin sydänprofiili ei eroa muiden uuden sukupolven antipsykoottien profiilista.
Aripipratsoli
Sillä on antipsykoottinen vaikutus, joka on verrattavissa muihin epätyypillisiin aineisiin, mutta sillä on suurempi vaikutus skitsofreniapotilaiden kognitiivisen toiminnan parametreihin. Edellä mainittu lääkkeen ainutlaatuinen farmakologinen vaikutus - D2-reseptorien osittainen agonisti - mahdollistaa ekstrapyramidaalisten oireyhtymien ja hyperprolaktinemian riskin vähentämisen sitä käytettäessä.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Amisulpridi
Kuuluu substituoitujen bentsamidien luokkaan. Lääke sitoutuu selektiivisesti D2- ja D3-dopaminergisten reseptorien alatyyppeihin, eikä sillä ole affiniteettia D1-, D4- ja D5-alatyyppeihin eikä serotoniini-, H1-histamiini-, a1-adrenergisiin ja kolinergisiin reseptoreihin. Suurina annoksina käytettynä se salpaa postsynaptisia D2-reseptoreita. Pieninä annoksina sen disinhibitorinen vaikutus ilmenee presynaptisten D2- ja D3-reseptorien salpauksen kautta, minkä vuoksi sen käyttö on tehokasta myös negatiivisten oireiden hoidossa, vaikka se ei olekaan yhdistetty D2- ja serotoniinireseptorien antagonisti. Useiden tutkimusten tulokset osoittavat lääkkeen voimakkaan antipsykoottisen vaikutuksen suurina annoksina käytettynä, mikä on perinteisiä lääkkeitä parempi.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
