Lääketieteen asiantuntija
Uudet julkaisut
Katekoliamiinien synteesi, eritys ja aineenvaihdunta
Viimeksi tarkistettu: 06.07.2025

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Lisämunuaisen ydin tuottaa yhdisteitä, joiden rakenne on kaukana steroideista. Ne sisältävät 3,4-dihydroksifenyyli- (katekoli-) ytimen ja niitä kutsutaan katekoliamiineiksi. Näitä ovat adrenaliini, noradrenaliini ja dopamiini-beeta-hydroksityramiini.
Katekoliamiinien synteesijärjestys on melko yksinkertainen: tyrosiini → dihydroksifenyylialaniini (DOPA) → dopamiini → noradrenaliini → adrenaliini. Tyrosiini tulee elimistöön ruoan mukana, mutta sitä voi muodostua myös fenyylialaniinista maksassa fenyylialaniinihydroksylaasin vaikutuksesta. Tyrosiinin muuntumisen lopputuotteet kudoksissa ovat erilaisia. Lisämunuaisen ytimessä prosessi etenee adrenaliinin muodostumisvaiheeseen, sympaattisten hermojen päissä - noradrenaliiniin, ja joissakin keskushermoston neuroneissa katekoliamiinien synteesi päättyy dopamiinin muodostumiseen.
Tyrosiinin muuntumista DOPA:ksi katalysoi tyrosiinihydroksylaasi, jonka kofaktoreita ovat tetrahydrobiopteriini ja happi. Tämän entsyymin uskotaan rajoittavan koko katekoliamiinibiosynteesin nopeutta ja estävän sen toimintaa prosessin lopputuotteilla. Tyrosiinihydroksylaasi on katekoliamiinibiosynteesin säätelyvaikutusten pääasiallinen kohde.
DOPAn muuntumista dopamiiniksi katalysoi DOPA-dekarboksylaasientsyymi (kofaktori - pyridoksaalifosfaatti), joka on suhteellisen epäspesifinen ja dekarboksyloi muita aromaattisia L-aminohappoja. On kuitenkin viitteitä siitä, että katekoliamiinien synteesiä voitaisiin muokata muuttamalla tämän entsyymin aktiivisuutta. Joiltakin neuroneilta puuttuu entsyymejä dopamiinin jatkokonversioon, ja se on lopputuote. Toiset kudokset sisältävät dopamiinibeeta-hydroksylaasia (kofaktorit - kupari, askorbiinihappo ja happi), joka muuntaa dopamiinin noradrenaliiniksi. Lisämunuaisten ytimessä (mutta ei sympaattisten hermojen päissä) on fenyylietanoliamiinia - metyylitransferaasi, joka muodostaa adrenaliinia noradrenaliinista. Tässä tapauksessa S-adenosyylimetioniini toimii metyyliryhmien luovuttajana.
On tärkeää muistaa, että fenyylietanoliamiini-N-metyylitransferaasin synteesi indusoituu glukokortikoidien saapuessa ytimeen aivokuoresta porttilaskimojärjestelmän kautta. Tämä voi selittää sen, miksi kaksi eri umpieritysrauhasta on yhdistynyt samaan elimeen. Glukokortikoidien merkitystä adrenaliinin synteesille korostaa se, että noradrenaliinia tuottavat lisämunuaisytimen solut sijaitsevat valtimoiden ympärillä, kun taas adrenaliinia tuottavat solut saavat verta pääasiassa lisämunuaisen kuoressa sijaitsevista laskimoiden poskionteloista.
Katekoliamiinien hajoaminen tapahtuu pääasiassa kahden entsyymijärjestelmän vaikutuksesta: katekoli-O-metyylitransferaasin (COMT) ja monoamiinioksidaasin (MAO). Adrenaliinin ja noradrenaliinin hajoamisen pääasialliset reitit on esitetty kaaviomaisesti kuvassa 54. COMT:n vaikutuksesta ja metyyliryhmädonorin S-adrenosyylimetioniinin läsnä ollessa katekoliamiinit muuttuvat normetanefriiniksi ja metanefriiniksi (noradrenaliinin ja adrenaliinin 3-O-metyylijohdannaiset), jotka MAO:n vaikutuksesta muuttuvat aldehydeiksi ja sitten (aldehydioksidaasin läsnä ollessa) vanillyylimantelihapoksi (VMA), joka on noradrenaliinin ja adrenaliinin tärkein hajoamistuote. Samassa tapauksessa, kun katekoliamiinit altistetaan aluksi MAO:lle COMT:n sijaan, ne muuttuvat 3,4-dioksomandeelialdehydiksi ja sitten aldehydioksidaasin ja COMT:n vaikutuksesta 3,4-dioksomandeelihapoksi ja VMC:ksi. Alkoholidehydrogenaasin läsnä ollessa katekoliamiineista voi muodostua 3-metoksi-4-oksifenyyliglykolia, joka on adrenaliinin ja noradrenaliinin hajoamisen pääasiallinen lopputuote keskushermostossa.
Dopamiinin hajoaminen on samanlaista, paitsi että sen metaboliiteista puuttuu hydroksyyliryhmä beeta-hiiliatomissa, ja siksi vanillyylimantelihapon sijaan muodostuu homovanilliinihappoa (HVA) eli 3-metoksi-4-hydroksifenyylietikkahappoa.
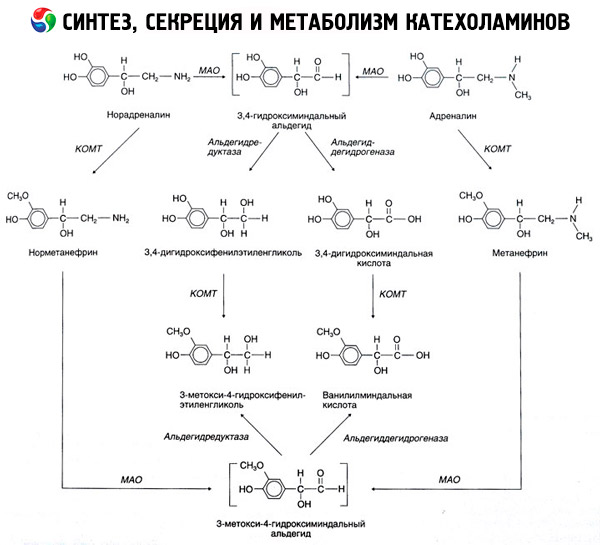
Katekolamiinimolekyylin hapettumiselle on myös oletettu kinoidinen reitti, joka voi tuottaa välituotteita, joilla on voimakas biologinen aktiivisuus.
Sympaattisten hermopäätteiden ja lisämunuaisen ytimessä sytosolisten entsyymien vaikutuksesta muodostuvat noradrenaliini ja adrenaliini kulkeutuvat erittävien rakeiden sisään, mikä suojaa niitä hajottavien entsyymien toiminnalta. Katekolamiinien sitominen rakeisiin vaatii energiankulutusta. Lisämunuaisen ytimen kromaffiinrakeissa katekoliamiinit ovat tiukasti sitoutuneet ATP:hen (suhteessa 4:1) ja spesifisiin proteiineihin - kromograniineihin, mikä estää hormonien diffuusion rakeista sytoplasmaan.
Katekolamiinien erityksen suora ärsyke on ilmeisesti kalsiumin tunkeutuminen soluun, mikä stimuloi eksosytoosia (rakeisen kalvon fuusio solun pintaan ja niiden repeäminen liukoisen sisällön - katekoliamiinien, dopamiini-beeta-hydroksylaasin, ATP:n ja kromograniinien - täydellisen vapautumisen myötä solunulkoiseen nesteeseen).
Katekoliamiinien fysiologiset vaikutukset ja niiden vaikutusmekanismi
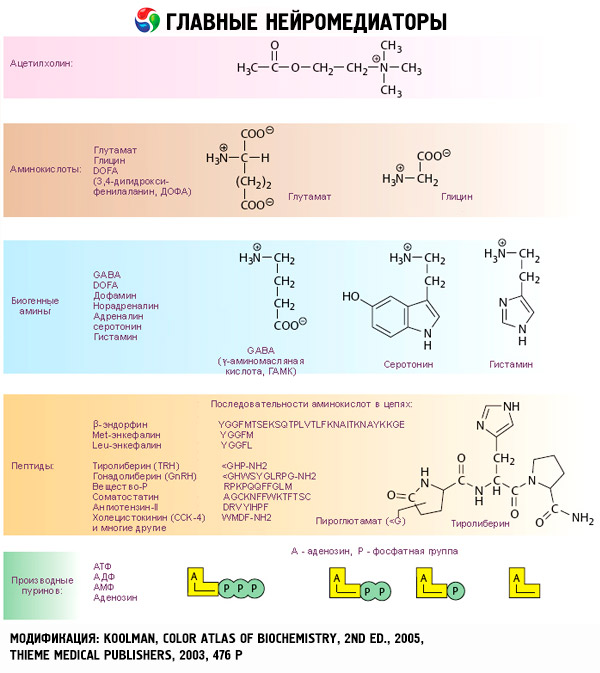
Katekolamiinien vaikutukset alkavat vuorovaikutuksesta kohdesolujen spesifisten reseptorien kanssa. Kilpirauhas- ja steroidihormonien reseptorit sijaitsevat solujen sisällä, kun taas katekoliamiinien (sekä asetyylikoliinin ja peptidihormonien) reseptorit sijaitsevat solun ulkopinnalla.
On jo pitkään tiedetty, että joissakin reaktioissa adrenaliini tai noradrenaliini ovat tehokkaampia kuin synteettinen katekoliamiini isoproterenoli, kun taas toisissa isoproterenolin vaikutus on adrenaliinin tai noradrenaliinin vaikutusta parempi. Tämän perusteella kehitettiin käsitys kahdenlaisten adrenoreseptorien esiintymisestä kudoksissa: alfa- ja beeta-adrenoreseptoreissa, ja joissakin niistä voi olla läsnä vain toinen näistä kahdesta tyypistä. Isoproterenoli on tehokkain beeta-adrenoreseptorien agonisti, kun taas synteettinen yhdiste fenyyliefriini on tehokkain alfa-adrenoreseptorien agonisti. Luonnolliset katekoliamiinit – adrenaliini ja noradrenaliini – pystyvät vuorovaikuttamaan molempien reseptorien kanssa, mutta adrenaliinilla on suurempi affiniteetti beeta- ja noradrenaliinilla alfa-reseptoreihin.
Katekoliamiinit aktivoivat sydämen beeta-adrenergisiä reseptoreita voimakkaammin kuin sileän lihaksen beeta-reseptoreita, minkä ansiosta beeta-tyyppi voidaan jakaa alatyyppeihin: beeta1-reseptorit (sydän, rasvasolut) ja beeta2-reseptorit (keuhkoputket, verisuonet jne.). Isoproterenolin vaikutus beeta1-reseptoreihin ylittää adrenaliinin ja noradrenaliinin vaikutuksen vain 10 kertaa, kun taas beeta2-reseptoreihin se vaikuttaa 100–1000 kertaa voimakkaammin kuin luonnolliset katekoliamiinit.
Spesifisten antagonistien (fentolamiini ja fenoksibentsamiini alfa- ja propranololi beeta-reseptoreille) käyttö vahvisti adrenoreseptorien luokittelun riittävyyden. Dopamiini kykenee vuorovaikuttamaan sekä alfa- että beeta-reseptorien kanssa, mutta myös eri kudoksilla (aivot, aivolisäke, verisuonet) on omia dopamiinireseptoreitaan, joiden spesifinen salpaaja on haloperidoli. Beeta-reseptorien määrä vaihtelee 1000:sta 2000:een solua kohden. Beeta-reseptorien välittämien katekoliamiinien biologiset vaikutukset liittyvät yleensä adenylaattisyklaasin aktivoitumiseen ja cAMP:n solunsisäisen pitoisuuden lisääntymiseen. Vaikka reseptori ja entsyymi ovat toiminnallisesti yhteydessä toisiinsa, ne ovat eri makromolekyylejä. Guanosiinitrifosfaatti (GTP) ja muut puriininukleotidit osallistuvat adenylaattisyklaasin aktiivisuuden modulointiin hormoni-reseptorikompleksin vaikutuksesta. Lisäämällä entsyymiaktiivisuutta ne näyttävät vähentävän beeta-reseptorien affiniteettia agonisteihin.
Denervoittuneiden rakenteiden lisääntyneen herkkyyden ilmiö on tunnettu jo pitkään. Päinvastoin, pitkäaikainen altistuminen agonisteille vähentää kohdekudosten herkkyyttä. Beeta-reseptorien tutkimus on mahdollistanut näiden ilmiöiden selittämisen. On osoitettu, että pitkäaikainen altistuminen isoproterenolille johtaa adenylaattisyklaasin herkkyyden menetykseen beeta-reseptorien määrän vähenemisen vuoksi.
Herkistysprosessi ei vaadi proteiinisynteesin aktivaatiota ja johtuu todennäköisesti peruuttamattomien hormoni-reseptorikompleksien asteittaisesta muodostumisesta. Päinvastoin, sympaattisia päätteitä tuhoavan 6-oksidopamiinin käyttöönottoon liittyy reagoivien beeta-reseptorien määrän kasvu kudoksissa. On mahdollista, että sympaattisen hermoston aktiivisuuden lisääntyminen aiheuttaa myös ikään liittyvää verisuonten ja rasvakudoksen herkistymistä katekoliamiineille.
Eri elinten adrenoreseptorien määrää voidaan säädellä muilla hormoneilla. Siten estradioli lisää ja progesteroni vähentää alfa-adrenoreseptorien määrää kohdussa, mihin liittyy vastaava lisääntyminen ja väheneminen niiden supistumisvasteessa katekoliamiineille. Jos beeta-reseptoriagonistien vaikutuksesta muodostuva solunsisäinen "toinen lähetti" on varmasti cAMP, niin tilanne alfa-adrenergisten vaikutusten välittäjäaineen suhteen on monimutkaisempi. Oletetaan useiden mekanismien olemassaoloa: cAMP-tason lasku, cAMP-pitoisuuden nousu, solun kalsiumdynamiikan modulointi jne.
Erilaisten vaikutusten toistamiseksi kehossa tarvitaan yleensä adrenaliiniannoksia, jotka ovat 5–10 kertaa pienempiä kuin noradrenaliini. Vaikka jälkimmäinen on tehokkaampi sekä alfa- että beeta1-adrenoreseptoreihin, on tärkeää muistaa, että molemmat endogeeniset katekoliamiinit kykenevät vuorovaikuttamaan sekä alfa- että beeta1-reseptorien kanssa. Siksi tietyn elimen biologinen vaste adrenergiseen aktivaatioon riippuu suurelta osin siinä olevien reseptorien tyypistä. Tämä ei kuitenkaan tarkoita, että sympaattisen-lisämunuaisjärjestelmän hermostollisen tai humoraalisen linkin selektiivinen aktivaatio olisi mahdotonta. Useimmissa tapauksissa havaitaan sen eri linkkien lisääntynyttä aktiivisuutta. Näin ollen on yleisesti hyväksyttyä, että hypoglykemia aktivoi refleksinomaisesti lisämunuaisytimen, kun taas verenpaineen laskuun (posturaalinen hypotensio) liittyy pääasiassa noradrenaliinin vapautuminen sympaattisten hermojen päistä.
Adrenoreseptorit ja niiden aktivaation vaikutukset eri kudoksissa
Järjestelmä, elin |
Adrenergisen reseptorin tyyppi |
Reaktio |
Sydän- ja verisuonijärjestelmä: |
||
Sydän |
Beeta |
Lisääntynyt syke, johtavuus ja supistuvuus |
Arteriolit: |
||
Iho ja limakalvot |
Alfa |
Vähennys |
Luustolihakset |
Beeta |
Laajeneminen Supistuminen |
Vatsan elimet |
Alfa (lisää) |
Vähennys |
Beeta |
Laajennus |
|
Suonet |
Alfa |
Vähennys |
Hengityselimet: |
||
Keuhkoputkien lihakset |
Beeta |
Laajennus |
Ruoansulatusjärjestelmä: |
||
Vatsa |
Beeta |
Heikentyneet motoriset taidot |
Suolet |
Alfa |
Sulkijalihasten supistuminen |
Perna |
Alfa |
Vähennys |
Beeta |
Rentoutuminen |
|
Eksokriininen haima |
Alfa |
Vähentynyt eritys |
Urogenitaalijärjestelmä: |
Alfa |
Sulkijalihaksen supistuminen |
Virtsarakko |
Beeta |
Ejektorilihaksen rentoutuminen |
Miehen sukuelimet |
Alfa |
Siemensyöksy |
Silmät |
Alfa |
Pupillin laajeneminen |
Nahka |
Alfa |
Lisääntynyt hikoilu |
Sylkirauhaset |
Alfa |
Kaliumin ja veden erittyminen |
Beeta |
Amylaasin eritys |
|
Umpieritysrauhaset: |
||
Haiman saarekkeet |
||
Beetasolut |
Alfa (lisää) |
Vähentynyt insuliinieritys |
Beeta |
Lisääntynyt insuliinin eritys |
|
Alfa-solut |
Beeta |
Lisääntynyt glukagonin eritys |
8-kennoinen |
Beeta |
Lisääntynyt somatostatiinin eritys |
Hypotalamus ja aivolisäke: |
||
Somatotrofit |
Alfa |
Lisääntynyt STH:n eritys |
Beeta |
STH:n erityksen väheneminen |
|
Laktotrofit |
Alfa |
Prolaktiinin erityksen väheneminen |
Tyreotrofit |
Alfa |
Vähentynyt TSH:n eritys |
Kortikotrofit |
Alfa |
Lisääntynyt ACTH-eritys |
| beeta | Vähentynyt ACTH-eritys | |
Kilpirauhanen: |
||
Follikulaariset solut |
Alfa |
Tyroksiinin erityksen väheneminen |
Beeta |
Lisääntynyt tyroksiinin eritys |
|
Parafollikulaariset (K) solut |
Beeta |
Lisääntynyt kalsitoniinin eritys |
Lisäkilpirauhaset |
Beeta |
Lisääntynyt PTH:n eritys |
Munuaiset |
Beeta |
Lisääntynyt reniinin eritys |
Vatsa |
Beeta |
Lisääntynyt gastriinin eritys |
BX |
Beeta |
Lisääntynyt hapenkulutus |
Maksa |
? |
Lisääntynyt glykogenolyysi ja glukoneogeneesi glukoosin vapautumisen myötä; lisääntynyt ketogeneesi ketoaineiden vapautumisen myötä |
Rasvakudos |
Beeta |
Lisääntynyt lipolyysi vapaiden rasvahappojen ja glyserolin vapautumisen myötä |
Luustolihakset |
Beeta |
Lisääntynyt glykolyysi pyruvaatin ja laktaatin vapautumisen myötä; vähentynyt proteolyysi alaniinin ja glutamiinin vapautumisen vähenemisen myötä |
On tärkeää ottaa huomioon, että katekoliamiinien laskimonsisäisen annon tulokset eivät aina heijasta riittävästi endogeenisten yhdisteiden vaikutuksia. Tämä pätee pääasiassa noradrenaliiniin, koska elimistössä sitä ei vapaudu pääasiassa vereen, vaan suoraan synaptisiin rakoihin. Siksi endogeeninen noradrenaliini aktivoi esimerkiksi paitsi verisuonten alfa-reseptoreita (kohonnut verenpaine), myös sydämen beeta-reseptoreita (kohonnut syke), kun taas ulkopuolelta tulevan noradrenaliinin anto johtaa pääasiassa verisuonten alfa-reseptorien aktivoitumiseen ja refleksinomaiseen (vagushermon kautta) sydämen sykkeen hidastumiseen.
Pienet adrenaliiniannokset aktivoivat pääasiassa lihasverisuonten ja sydämen beetareseptoreita, mikä johtaa perifeerisen verisuonten vastuksen vähenemiseen ja sydämen minuuttitilavuuden lisääntymiseen. Joissakin tapauksissa ensimmäinen vaikutus voi vallita, ja adrenaliinin annon jälkeen kehittyy hypotensio. Suuremmilla annoksilla adrenaliini aktivoi myös alfareseptoreita, johon liittyy perifeerisen verisuonten vastuksen lisääntyminen ja sydämen minuuttitilavuuden lisääntymisen taustalla johtaa valtimopaineen nousuun. Sen vaikutus verisuonten beetareseptoreihin säilyy kuitenkin myös. Tämän seurauksena systolisen paineen nousu ylittää vastaavan diastolisen paineen (pulssin paineen nousun). Vielä suurempien annosten käyttöönoton myötä adrenaliinin alfamimeettiset vaikutukset alkavat vallita: systolinen ja diastolinen paine nousevat rinnakkain, kuten noradrenaliinin vaikutuksesta.
Katekoliamiinien vaikutus aineenvaihduntaan koostuu niiden suorista ja epäsuorista vaikutuksista. Ensimmäiset toteutuvat pääasiassa beeta-reseptorien kautta. Monimutkaisemmat prosessit liittyvät maksaan. Vaikka lisääntynyttä maksan glykogenolyysiä pidetään perinteisesti beeta-reseptorien aktivaation seurauksena, on myös näyttöä alfa-reseptorien osallisuudesta. Katekoliamiinien epäsuorat vaikutukset liittyvät monien muiden hormonien, kuten insuliinin, erityksen säätelyyn. Adrenaliinin vaikutuksessa sen eritykseen alfa-adrenerginen komponentti on selvästi vallitseva, koska on osoitettu, että mihin tahansa stressiin liittyy insuliinin erityksen estyminen.
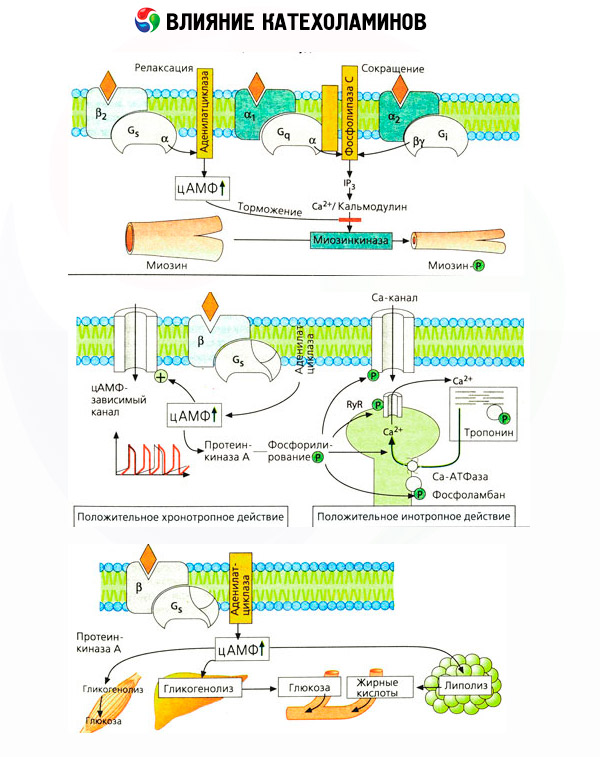
Katekoliamiinien suorien ja epäsuorien vaikutusten yhdistelmä aiheuttaa hyperglykemiaa, joka liittyy paitsi lisääntyneeseen maksan glukoosin tuotantoon, myös sen käytön estymiseen ääreiskudoksissa. Lipolyysin kiihtyminen aiheuttaa hyperlipidemiaa, mikä lisää rasvahappojen kulkeutumista maksaan ja tehostaa ketoaineiden tuotantoa. Lisääntynyt glykolyysi lihaksissa johtaa laktaatin ja pyruvaatin vapautumisen lisääntymiseen vereen, jotka yhdessä rasvakudoksesta vapautuvan glyserolin kanssa toimivat maksan glukoneogeneesin esiasteina.
Katekolamiinien erityksen säätely. Sympaattisen hermoston ja lisämunuaisen ytimen tuotteiden ja reaktiomenetelmien samankaltaisuus oli perusta näiden rakenteiden yhdistämiselle yhdeksi kehon sympaattisen-lisämunuaisen järjestelmäksi hermostollisten ja hormonaalisten yhteyksien jakautumisella. Hypotalamukseen ja selkäytimen ja ytimen keskuksiin keskittyy erilaisia afferenttisignaaleja, joista efferentit viestit lähtevät ja siirtyvät selkäytimen sivusarveissa sijaitsevien preganglionisten neuronien solukappaleisiin VIII-kaula-II-III lannerangan segmenttien tasolla.
Näiden solujen preganglionaariset aksonit poistuvat selkäytimestä ja muodostavat synaptisia yhteyksiä sympaattisen ketjun ganglioissa sijaitsevien hermosolujen tai lisämunuaisen ytimen solujen kanssa. Nämä preganglionaariset kuidut ovat kolinergisiä. Ensimmäinen perustavanlaatuinen ero sympaattisten postganglionaaristen hermosolujen ja lisämunuaisen ytimen kromaffiinisolujen välillä on se, että jälkimmäiset välittävät vastaanottamansa kolinergisen signaalin hermojohtumisen (postganglionaariset adrenergiset hermot) sijaan humoraalista reittiä pitkin vapauttaen adrenergisiä yhdisteitä vereen. Toinen ero on se, että postganglionaariset hermot tuottavat noradrenaliinia, kun taas lisämunuaisen ytimen solut tuottavat pääasiassa adrenaliinia. Näillä kahdella aineella on erilaiset vaikutukset kudoksiin.

