Lääketieteen asiantuntija
Uudet julkaisut
Nivelrikon diagnosointi: magneettikuvaus
Viimeksi tarkistettu: 04.07.2025

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
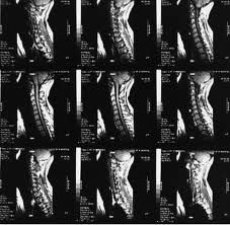
Magneettikuvaus (MRI) on viime vuosina noussut yhdeksi johtavista nivelrikon ei-invasiivisista diagnostiikkamenetelmistä. 1970-luvulta lähtien, jolloin magneettikuvauksen (MRI) periaatteita alettiin ensimmäisen kerran käyttää ihmiskehon tutkimiseen, tämä lääketieteellisen kuvantamisen menetelmä on muuttunut dramaattisesti ja kehittyy edelleen nopeasti.
Teknisiä laitteita ja ohjelmistoja parannetaan, kuvantamismenetelmiä kehitetään ja magneettikuvausvarjoaineita kehitetään. Tämä mahdollistaa magneettikuvauksen jatkuvasti uusien sovellusalueiden löytämisen. Jos aluksi sen käyttö rajoittui keskushermoston tutkimuksiin, nyt magneettikuvausta käytetään menestyksekkäästi lähes kaikilla lääketieteen aloilla.
Vuonna 1946 Stanfordin ja Harvardin yliopistojen tutkijaryhmät löysivät itsenäisesti ilmiön nimeltä ydinmagneettinen resonanssi (NMR). Sen ydin oli se, että joidenkin atomien ytimet, jotka ovat magneettikentässä ulkoisen sähkömagneettisen kentän vaikutuksen alaisina, kykenevät absorboimaan energiaa ja sitten lähettämään sen radiosignaalin muodossa. Tästä löydöstä F. Bloch ja E. Parmel saivat Nobel-palkinnon vuonna 1952. Uutta ilmiötä käytettiin pian biologisten rakenteiden spektrianalyysiin (NMR-spektroskopia). Vuonna 1973 Paul Rautenburg osoitti ensimmäisenä mahdollisuuden saada kuva NMR-signaalien avulla. Näin NMR-tomografia syntyi. Ensimmäiset elävän ihmisen sisäelinten NMR-tomogrammit esiteltiin vuonna 1982 Pariisin kansainvälisessä radiologien kongressissa.
Kaksi selvennystä on syytä antaa. Vaikka menetelmä perustuu NMR-ilmiöön, sitä kutsutaan magneettiresonanssiksi (MR), josta sana "ydinvoima" jätetään pois. Tämä tehdään, jotta potilailla ei olisi ajatuksia atomiytimien hajoamiseen liittyvästä radioaktiivisuudesta. Ja toinen seikka: MR-tomografeja ei vahingossa "viritetä" protoneille eli vetyytimille. Tätä alkuainetta on paljon kudoksissa, ja sen ytimillä on kaikista atomiytimistä suurin magneettinen momentti, mikä määrää melko korkean MR-signaalin tason.
Jos vuonna 1983 maailmassa oli vain muutamia kliiniseen tutkimukseen soveltuvia laitteita, niin vuoden 1996 alkuun mennessä maailmanlaajuisesti oli käytössä noin 10 000 tomografia. Joka vuosi käyttöön otetaan 1000 uutta laitetta. Yli 90 % magneettikuvauslaitteiden parista on malleja, joissa on suprajohtavat magneetit (0,5–1,5 T). On mielenkiintoista huomata, että jos 1980-luvun puolivälissä magneettikuvauslaitteiden valmistajat noudattivat periaatetta "mitä suurempi kenttä, sitä parempi" ja keskittyivät malleihin, joiden kenttä oli 1,5 T tai enemmän, niin 1980-luvun loppuun mennessä kävi selväksi, että useimmilla sovellusalueilla niillä ei ole merkittäviä etuja malleihin verrattuna, joilla on keskimääräinen kentänvoimakkuus. Siksi MR-tomografien päävalmistajat (General Electric, Siemens, Philips, Toshiba, Picker, Bruker jne.) kiinnittävät tällä hetkellä paljon huomiota keski- ja jopa matalakenttien mallien tuotantoon, jotka eroavat korkeakentäisistä järjestelmistä kompaktiutensa ja taloudellisuutensa ansiosta tyydyttävällä kuvanlaadulla ja huomattavasti alhaisemmilla kustannuksilla. Korkeakentäisiä järjestelmiä käytetään pääasiassa tutkimuskeskuksissa MR-spektroskopiaan.
MRI-menetelmän periaate
Magneettikuvauslaitteen pääkomponentit ovat: erittäin voimakas magneetti, radiolähetin, vastaanottava radiotaajuuskäämi, tietokone ja ohjauspaneeli. Useimmissa laitteissa on magneettikenttä, jonka magneettinen momentti on ihmiskehon pituusakselin suuntainen. Magneettikentän voimakkuus mitataan tesloina (T). Kliinisessä magneettikuvauksessa käytetään 0,2–1,5 T:n voimakkuuden omaavia kenttiä.
Kun potilas asetetaan voimakkaaseen magneettikenttään, kaikki protonit, jotka ovat magneettisia dipoleja, kääntyvät ulkoisen kentän suuntaan (kuten kompassin neula, joka on suunnattu kohti maan magneettikenttää). Lisäksi jokaisen protonin magneettinen akseli alkaa pyöriä ulkoisen magneettikentän suunnan ympäri. Tätä tiettyä pyörimisliikettä kutsutaan kulkueeksi ja sen taajuutta resonanssitaajuudeksi. Kun lyhyitä sähkömagneettisia radiotaajuuspulsseja johdetaan potilaan kehon läpi, radioaaltojen magneettikenttä saa kaikkien protonien magneettiset momentit pyörimään ulkoisen kentän magneettisen momentin ympäri. Jotta tämä tapahtuisi, radioaaltojen taajuuden on oltava yhtä suuri kuin protonien resonanssitaajuus. Tätä ilmiötä kutsutaan magneettiresonanssiksi. Magneettisten protonien suunnan muuttamiseksi protonien ja radioaaltojen magneettikenttien on resonoitava eli oltava samalla taajuudella.
Potilaan kudoksiin syntyy magneettinen nettomomentti: kudokset magnetoituvat ja niiden magnetismi on suunnattu täysin ulkoisen magneettikentän suuntaisesti. Magnetismi on verrannollinen protonien määrään kudostilavuusyksikköä kohti. Useimmissa kudoksissa olevien protonien (vetyytimien) valtava määrä tarkoittaa, että magneettinen nettomomentti on riittävän suuri indusoimaan sähkövirran potilaan ulkopuolella sijaitsevaan vastaanottokäämiin. Näitä indusoituja magneettikuvaussignaaleja käytetään magneettikuvan rekonstruointiin.
Ytimen elektronien siirtymistä viritystilasta tasapainotilaan kutsutaan spin-hila-relaksaatioprosessiksi eli pitkittäiseksi relaksaatioksi. Sille on tunnusomaista T1 - spin-hila-relaksaatioaika - aika, joka kuluu 63 %:n ytimien siirtymiseen tasapainotilaan 90°:n virityksen jälkeen. T2 - spin-spin-relaksaatioaika - erotetaan myös toisistaan.
Magneettikuvausten ottamiseksi on useita menetelmiä. Ne eroavat toisistaan radiotaajuuspulssien generoinnin järjestyksen ja luonteen sekä magneettikuvaussignaalin analyysimenetelmien suhteen. Kaksi yleisimmin käytettyä menetelmää ovat spin-lattice ja spin-echo. Spin-lattice analysoi pääasiassa T1-relaksaatioaikaa. Eri kudokset (aivojen harmaa ja valkea aine, aivo-selkäydinneste, kasvainkudos, rusto, lihakset jne.) sisältävät protoneja, joilla on erilaiset T1-relaksaatioajat. Magneettikuvauksen intensiteetti liittyy T1:n kestoon: mitä lyhyempi T1 on, sitä voimakkaampi MR-signaali on ja sitä kirkkaampi kuvan tietty alue näkyy TV-näytössä. Rasvakudos on valkoista magneettikuvauksissa, jota seuraavat aivot ja selkäydin, tiheät sisäelimet, verisuonten seinämät ja lihakset magneettikuvauksen intensiteetin laskevassa järjestyksessä. Ilma, luut ja kalkkeutumat eivät käytännössä tuota magneettikuvausta, ja siksi ne näkyvät mustina. Nämä T1-relaksaatioaikasuhteet luovat edellytykset normaalien ja muuttuneiden kudosten visualisoinnille magneettikuvauksissa.
Toisessa magneettikuvausmenetelmässä, spin-kaikumenetelmässä, potilaaseen kohdistetaan sarja radiotaajuuspulsseja, jotka pyörittävät liikkuvia protoneja 90°. Pulssien loppumisen jälkeen magneettikuvausvastesignaalit tallennetaan. Vastesignaalin voimakkuus riippuu kuitenkin T2-ajan kestosta eri tavalla: mitä lyhyempi T2, sitä heikompi signaali ja sitä pienempi TV-näytön hehkun kirkkaus. Siten lopullinen magneettikuvaus T2-menetelmällä on päinvastainen kuin T1-menetelmällä (koska negatiivinen on positiivisen vastakohta).
Magneettikuvaukset näyttävät pehmytkudokset paremmin kuin tietokonetomografiakuvat: lihakset, rasvakerrokset, ruston ja verisuonet. Jotkut laitteet voivat tuottaa kuvia verisuonista ilman varjoaineen injektoimista (magneettiangiografia). Luukudosten alhaisen vesipitoisuuden vuoksi varjoaine ei luo suojaavaa vaikutusta, kuten röntgen-TT-kuvauksessa, eli se ei häiritse esimerkiksi selkäytimen, nikamien välisten välilevyjen jne. kuvaa. Vetyytimet eivät tietenkään ole vain vedessä, vaan luukudoksessa ne ovat kiinnittyneet erittäin suuriin molekyyleihin ja tiheisiin rakenteisiin eivätkä häiritse magneettikuvausta.
MRI:n edut ja haitat
Magneettikuvauksen (MRI) tärkeimpiä etuja ovat ei-invasiivinen, vaaraton (ei säteilyaltistusta), kuvantamisen kolmiulotteinen luonne, luonnollinen kontrasti liikkuvasta verestä, luukudoksesta peräisin olevien artefaktien puuttuminen, pehmytkudosten korkea erilaistuminen sekä kyky suorittaa MP-spektroskopiaa kudosaineenvaihdunnan in vivo -tutkimuksia varten. Magneettikuvauksella voidaan saada kuvia ihmiskehon ohuista kerroksista missä tahansa osassa - otsa-, sagittaali-, aksiaali- ja vinossa tasossa. On mahdollista rekonstruoida elinten volumetrisia kuvia ja synkronoida tomogrammien ottaminen EKG:n hampaiden kanssa.
Tärkeimpiin haittoihin kuuluvat yleensä kuvien saamiseen kuluva suhteellisen pitkä aika (yleensä minuutteja), mikä johtaa hengitysliikkeistä aiheutuvien artefaktien esiintymiseen (tämä erityisesti heikentää keuhkojen tutkimuksen tehokkuutta), rytmihäiriöt (sydäntutkimuksessa), kyvyttömyys havaita luotettavasti kiviä, kalkkeutumista, tietyntyyppisiä luupatologioita, laitteiden ja niiden käytön korkeat kustannukset, erityisvaatimukset tiloille, joissa laitteet sijaitsevat (häiriösuojaus), kyvyttömyys tutkia klaustrofobiasta kärsiviä potilaita, keinotekoiset sydämentahdistimet, suuret metalli-implantit, jotka on valmistettu ei-lääketieteellisistä metalleista.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
MRI-kontrastiaineet
Magneettikuvauksen käytön alkuaikoina uskottiin, että eri kudosten välinen luonnollinen kontrasti eliminoi varjoaineiden tarpeen. Pian havaittiin, että varjoaineilla voitiin parantaa merkittävästi eri kudosten välisten signaalien eroa eli magneettikuvan kontrastia. Kun ensimmäinen magneettikuvauksen varjoaine (joka sisälsi paramagneettisia gadoliniumi-ioneja) tuli kaupallisesti saataville, magneettikuvauksen diagnostinen informaatiosisältö kasvoi merkittävästi. Magneettikuvauksen varjoaineiden käytön ydin on kudos- ja elinprotonien magneettisten parametrien muuttaminen eli T1- ja T2-protonien relaksaatioajan (TR) muuttaminen. Nykyään magneettikuvauksen varjoaineita (tai pikemminkin varjoaineita - CA) on useita luokituksia.
Rentoutumisaikaan kohdistuvan vallitsevan vaikutuksen mukaan MR-KA jaetaan seuraavasti:
- T1-CA, jotka lyhentävät T1:tä ja siten lisäävät kudoksen MP-signaalin voimakkuutta. Niitä kutsutaan myös positiivisiksi CA:iksi.
- T2-CA:t, jotka lyhentävät T2:ta ja vähentävät MR-signaalin voimakkuutta. Nämä ovat negatiivisia CA:ita.
Magneettisten ominaisuuksiensa perusteella MR-CA jaetaan paramagneettisiin ja superparamagneettisiin:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Paramagneettiset varjoaineet
Paramagneettisia ominaisuuksia on atomeilla, joilla on yksi tai useampi pariton elektroni. Nämä ovat gadoliniumin (Gd), kromin, nikkelin, raudan ja mangaanin magneettisia ioneja. Gadoliniumyhdisteet ovat saaneet laajimman kliinisen käytön. Gadoliniumin kontrastivaikutus johtuu relaksaatioaikojen T1 ja T2 lyhenemisestä. Pienillä annoksilla vaikutus T1:een on vallitseva, mikä lisää signaalin voimakkuutta. Suurilla annoksilla vaikutus T2:een on vallitseva, mikä vähentää signaalin voimakkuutta. Paramagneettisia aineita käytetään nykyään laajimmin kliinisessä diagnostiikassa.
Superparamagneettiset varjoaineet
Superparamagneettisen rautaoksidin hallitseva vaikutus on T2-relaksaation lyheneminen. Annoksen kasvaessa signaalin voimakkuus heikkenee. Tähän rautaoksidiryhmään voidaan myös lukea ferromagneettisia rautaoksideja, jotka ovat rakenteellisesti samanlaisia kuin magnetiittiferriitti ( Fe2+ OFe23 + O3 ) .
Seuraava luokittelu perustuu CA:n farmakokinetiikkaan (Sergeev PV et al., 1995):
- solunulkoinen (kudoskohtainen);
- ruoansulatuskanava;
- organotrooppinen (kudoskohtainen);
- makromolekyyliset, joita käytetään verisuonitilan määrittämiseen.
Ukrainassa tunnetaan neljä MR-CA:ta, jotka ovat solunulkoisia vesiliukoisia paramagneettisia CA:ita, joista gadodiamidia ja gadopenteettihappoa käytetään laajalti. Loput CA-ryhmät (2–4) ovat kliinisissä tutkimuksissa ulkomailla.
Solunulkoinen vesiliukoinen MR-CA
Kansainvälinen nimi |
Kemiallinen kaava |
Rakenne |
Gadopenteettihappo |
Gadoliniumdimeglumiinidietyleenitriamiinipenta-asetaatti ((NMG)2Gd-DTPA) |
Lineaarinen, ioninen |
Gadoteerihappo |
(NMG)Gd-DOTA |
Syklinen, ioninen |
Gadodiamidi |
Gadoliniumdietyleenitriamiinipenta-asetaatti-bis-metyyliamidi (Gd-DTPA-BMA) |
Lineaarinen, ioniton |
Gadoteridoli |
Gd-HP-D03A |
Syklinen, ioniton |
Solunulkoisia CA-yhdisteitä annetaan laskimonsisäisesti, 98 % niistä erittyy munuaisten kautta, eivät läpäise veri-aivoestettä, ovat vähämyrkyllisiä ja kuuluvat paramagneettisten aineiden ryhmään.
MRI-kuvauksen vasta-aiheet
Absoluuttisiin vasta-aiheisiin kuuluvat tilanteet, joissa tutkimus on uhka potilaiden hengelle. Esimerkiksi elektronisesti, magneettisesti tai mekaanisesti aktivoituvien implanttien läsnäolo – nämä ovat pääasiassa keinotekoisia sydämentahdistimia. Magneettikuvauslaitteen radiotaajuussäteilylle altistuminen voi häiritä pyyntöjärjestelmässä toimivan tahdistimen toimintaa, koska magneettikenttien muutokset voivat jäljitellä sydämen toimintaa. Magneettinen vetovoima voi myös aiheuttaa tahdistimen siirtymisen kannassaan ja elektrodien siirtämisen. Lisäksi magneettikenttä luo esteitä ferromagneettisten tai elektronisten välikorvaimplanttien toiminnalle. Keinotekoisten sydänläppien läsnäolo on vaarallinen ja ehdoton vasta-aihe vain silloin, kun niitä tutkitaan magneettikuvauslaitteilla, joissa on korkeat kentät, ja jos läpän vaurioitumista epäillään kliinisesti. Tutkimuksen absoluuttisiin vasta-aiheisiin kuuluvat myös pienten metallisten kirurgisten implanttien (verenvuodon tyrehdyttäjien) läsnäolo keskushermostossa, koska niiden siirtyminen magneettisen vetovoiman vuoksi uhkaa verenvuotoa. Niiden läsnäolo muissa kehon osissa on pienempi uhka, koska hoidon jälkeen fibroosi ja puristimien kapselointi auttavat pitämään ne vakaina. Mahdollisen vaaran lisäksi magneettisia ominaisuuksia omaavien metallisten implanttien läsnäolo aiheuttaa joka tapauksessa artefakteja, jotka vaikeuttavat tutkimustulosten tulkintaa.
MRI-kuvauksen vasta-aiheet
Absoluuttinen: |
Suhteellinen: |
Sydämentahdistimet |
Muut stimulantit (insuliinipumput, hermoja stimuloivat lääkkeet) |
Ferromagneettiset tai elektroniset välikorvaimplantit |
Ei-ferromagneettiset sisäkorvan implantit, sydänläppäproteesit (voimakkaissa kentissä, jos epäillään toimintahäiriötä) |
Aivoverisuonten hemostaattiset klipsit |
Verenvuodon tyrehdyttäjät muissa paikoissa, dekompensoitunut sydämen vajaatoiminta, raskaus, ahtaan paikan kammo, fysiologisen seurannan tarve |
Suhteellisia vasta-aiheita edellä mainittujen lisäksi ovat dekompensoitu sydämen vajaatoiminta ja fysiologisen seurannan tarve (mekaaninen ventilaatio, sähköiset infuusiopumput). Klaustrofobia on este tutkimukselle 1–4 %:ssa tapauksista. Se voidaan voittaa toisaalta käyttämällä laitteita, joissa on avoimet magneetit, ja toisaalta yksityiskohtaisella selityksellä laitteesta ja tutkimuksen kulusta. Magneettikuvauksen vahingollisesta vaikutuksesta alkioon tai sikiöön ei ole näyttöä, mutta magneettikuvauksen välttämistä suositellaan raskauden ensimmäisen kolmanneksen aikana. Magneettikuvauksen käyttö raskauden aikana on aiheellista tapauksissa, joissa muut ei-ionisoivat diagnostiset kuvantamismenetelmät eivät anna tyydyttävää tietoa. Magneettikuvaus vaatii enemmän potilaan osallistumista kuin tietokonetomografia, koska potilaan liikkeet tutkimuksen aikana vaikuttavat paljon enemmän kuvien laatuun, joten akuutista patologiasta, tajunnan heikkenemisestä, spastisista tiloista, dementiasta kärsivien potilaiden sekä lasten tutkiminen on usein vaikeaa.

