Tutkijat ovat löytäneet uuden immunosuppressiivisen mekanismin aivosyövässä
Viimeksi tarkistettu: 14.06.2024

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Apulaisprofessori Filippo Veglia, Ph.D., ja hänen tiiminsä Wistar Institutesta ovat löytäneet keskeisen mekanismin, jolla glioblastooma – vakava ja usein kuolemaan johtava aivosyöpä — tukahduttaa immuunijärjestelmän toimintaa niin, että kasvain voi kasvaa ilman, että kehon puolustusmekanismit vastustavat sitä.
Heidän löytönsä julkaistiin artikkelissa "Glukoosiohjattu histonin laktylaatio edistää monosyyttiperäisten makrofagien immunosuppressiivista aktiivisuutta glioblastoomassa" Immunity -julkaisussa.
"Tutkimuksemme osoittavat, että syövän itsensä säilymisen mekanismeja voidaan käyttää tautia vastaan erittäin tehokkaasti, jos niitä ymmärretään riittävästi", sanoi tohtori Veglia.
"Odotan innolla tulevaa tutkimusta metabolisen immunosuppression mekanismeista glioblastoomassa ja toivon, että opimme jatkossakin lisää tämän syövän ymmärtämisestä ja torjumisesta."
Tähän mennessä on tutkittu vähän siitä, kuinka monosyyteistä peräisin olevat makrofagit ja mikrogliat luovat immunosuppressiivisen kasvaimen mikroympäristön glioblastoomassa.
Weglian laboratorio tutki immunosuppression solumekanismeja glioblastoomassa ja havaitsi, että glioblastooman edetessä monosyyteistä peräisin olevat makrofagit alkavat ylittää mikroglioiden määrän, mikä osoittaa, että monosyyteistä peräisin olevien makrofagien vallitsevuus kasvaimen mikroympäristössä on hyödyllistä syövälle. Immuunivasteen välttäminen.
Monosyyteistä peräisin olevat makrofagit, mutta eivät mikrogliat, estivät T-solujen (tuumorisoluja tuhoavien immuunisolujen) toiminnan prekliinisissä malleissa ja potilaissa. Ryhmä vahvisti tämän arvioimalla prekliinisiä glioblastoomamalleja, joissa on keinotekoisesti vähennetty monosyyteistä peräisin olevien makrofagien määrää.
Odotusten mukaisesti mallit, joissa oli vähemmän pahanlaatuisia makrofageja kasvaimen mikroympäristössä, osoittivat parempia tuloksia verrattuna tavallisiin glioblastoomamalleihin.
Glioblastooma muodostaa hieman yli puolet kaikista aivoissa syntyvistä pahanlaatuisista kasvaimista, ja ennuste potilaille, joilla on diagnosoitu tämä sairaus, on erittäin huono: vain 25 % potilaista selviää ensimmäisen vuoden diagnoosin jälkeen. Glioblastooma ei ole vaarallinen vain sen sijainnin vuoksi aivoissa, vaan myös immunosuppressiivisen kasvainmikroympäristön vuoksi, mikä tekee glioblastoomasta vastustuskykyisen lupaaville immunohoidoille.
Ohjelmoimalla tietyt immuunisolut, kuten makrofagit (monosyyteistä peräisin olevat makrofagit ja mikrogliat) toimimaan kasvaimen hyväksi eikä sitä vastaan, glioblastooma luo itselleen kasvaimen mikroympäristön, joka sallii syövän kasvaa aggressiivisesti ja välttää syöpää vastaan. Immuunivasteet.
Mekanismin selvittäminen
Vahvistettuaan monosyyteistä peräisin olevien makrofagien roolin Weglian laboratorio yritti seuraavaksi ymmärtää tarkasti, kuinka nämä syöpään liittyvät immuunisolut toimivat immuunijärjestelmää vastaan.
He sekvensoivat makrofageja määrittääkseen, oliko soluissa epänormaaleja geenien ilmentymismalleja, jotka voisivat viitata geeneihin, joilla on rooli immunosuppressiossa, ja tutkivat myös makrofagien aineenvaihduntamalleja ymmärtääkseen, liittyikö epänormaali geenin ilmentyminen aineenvaihduntaan.
Geeni- ja aineenvaihdunta-analyysi johti ne glukoosiaineenvaihduntaan. Sarja kokeita osoitti, että monosyyteistä peräisin olevat makrofagit, joilla oli lisääntynyt glukoosin aineenvaihdunta ja GLUT1:n, pääasiallisen glukoosin kuljettajan, ilmentyminen, estivät T-solujen toiminnan vapauttamalla interleukiini-10:tä (IL-10).
Tiimi osoitti, että glioblastooma häiritsee glukoosin aineenvaihduntaa näissä makrofageissa, jolloin niistä tulee immunosuppressiivisia.
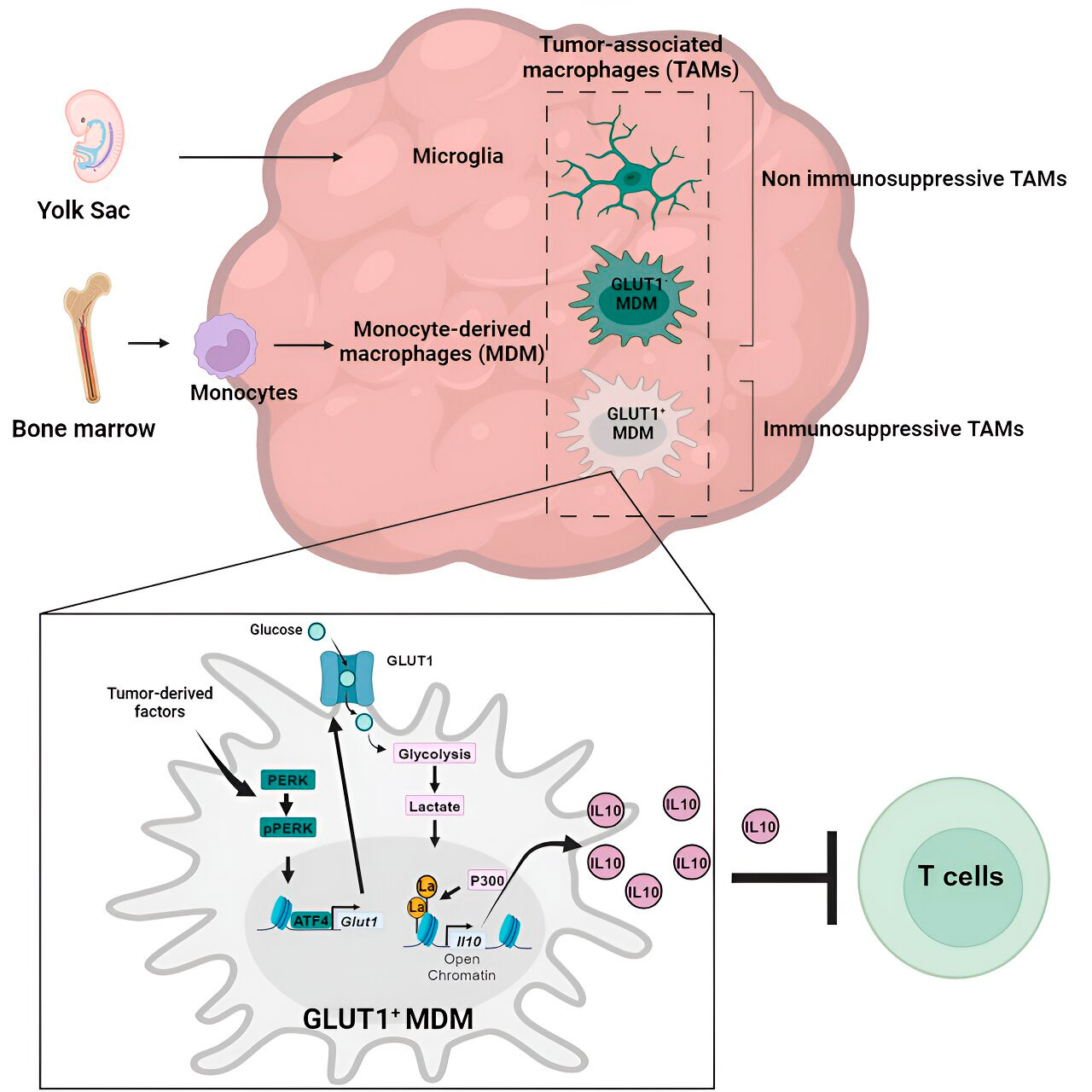
Histonilaktylaatio ja sen rooli
Tutkijat ovat havainneet, että avain glukoosiaineenvaihduntaan liittyvien monosyyteistä peräisin olevien makrofagien immunosuppressiiviseen toimintaan on prosessissa, jota kutsutaan "histonin laktylaatioksi". Histonit ovat genomin rakenneproteiineja, joilla on avainrooli geenien, kuten IL-10:n, ilmentymisessä tietyissä yhteyksissä.
Monosyyteistä peräisin olevat makrofagit tuottavat laktaattia, glukoosiaineenvaihdunnan sivutuotetta, metaboloimalla nopeasti glukoosia. Histonit voivat "laktyloitua" (eli laktaatti integroituu histoneihin), jolloin histoniorganisaatio edistää IL-10:n ilmentymistä, jota monosyyteistä peräisin olevat makrofagit tuottavat tukemaan syöpäsolujen kasvua.
Ongelman ratkaisu
Mutta kuinka voit pysäyttää glukoosiaineenvaihduntaan liittyvien monosyyteistä peräisin olevien makrofagien immunosuppressiivisen toiminnan? Tohtori Veglia ja hänen tiiminsä löysivät mahdollisen ratkaisun: PERK:n, entsyymin, jonka he tunnistivat glukoosiaineenvaihdunnan ja GLUT1:n ilmentymisen säätelijäksi makrofageissa.
Prekliinisissä glioblastoomamalleissa PERK:iin kohdistuminen häiritsi histonin laktylaatiota ja makrofagien immunosuppressiivista aktiivisuutta, ja yhdistettynä immunoterapian kanssa esti glioblastooman etenemisen ja aiheutti pitkäaikaisen immuniteetin, joka suojeli aivoja kasvaimen uudelleenkasvulta, mikä viittaa siihen, että PERK-histonin kohdistaminen laktylaatioakseli voi olla toteuttamiskelpoinen strategia tämän tappavan aivosyövän torjumiseksi.
