Uudet julkaisut
Tutkimus korostaa tarvetta solutyyppikohtaisille hoitomuodoille HIV:n hoidossa.
Viimeksi tarkistettu: 02.07.2025

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
Illinoisin yliopiston tutkijat ovat osoittaneet tiettyjen solutyyppien kohdentamisen tärkeyden HIV:n hoidossa. Heidän tutkimuksensa, joka julkaistiin Proceedings of the National Academy of Sciences -lehdessä, on yksi ensimmäisistä, joissa tarkastellaan HIV:n latenssimodulaation erilaistuneita tai solutyyppikohtaisia vaikutuksia myeloidisoluihin, jotka ovat luuytimessä tuotettavia immuunisoluja.
Yksi HIV-infektion eliminoinnin suurimmista esteistä on latenssiajan eli sen ajanjakson hallinta, jonka aikana tartunnan saanut solu on lepotilassa eikä pysty tuottamaan virusta. Latenttiset HIV-solut kerääntyvät kehoon paikkoihin, joita kutsutaan reservuareiksi. Latenttiset reservuaarit ovat ongelmallisia, koska ne voivat alkaa tuottaa virusta milloin tahansa.
Taudin täydellinen hävittäminen edellyttäisi kaikkien piilevien solujen poistamista kehosta tai pysyvää vastustuskykyä aktivaatioärsykkeille. Uudelleenaktivoitumisen voivat kuitenkin laukaista useat tekijät, mukaan lukien signaalit, jotka ohjaavat myeloidisolujen erilaistumista.
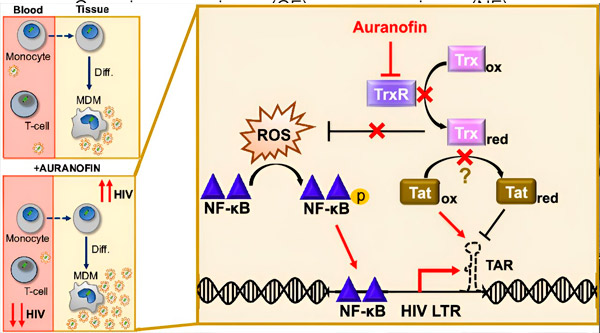
HIV-latenssin säätely monosyyteistä peräisin olevissa makrofageissa (MDM) voi aiheuttaa riskin viruksen leviämiselle. Monosyyttien erilaistuminen makrofageiksi voi laukaista HIV:n uudelleenaktivoitumisen, mikä voi edistää viruksen leviämistä kudoksiin (ylhäällä vasemmalla). Kliininen ehdokas, auranofiini, vähentää viruksen DNA:ta veressä ja edistää HIV:n latenssia T-soluissa ja monosyyteissä, mutta aiheuttaa HIV:n uudelleenaktivoitumisen MDM:issä (alhaalla vasemmalla). MDM:issä oletamme, että TrxR:n esto auranofiinilla johtaa reaktiivisten happilajien (ROS) kertymiseen, mikä indusoi NF-κB:n aktivaation ja HIV:n LTR-promoottorin aktivaation (oikealla). TrxR:n esto voi mahdollisesti vähentää substraattien pelkistymistä, jolloin Tat-proteiini pysyy ensisijaisesti hapettuneena, missä se voi sitoutua TAR:iin ja aloittaa HIV:n transkription. Lähde: Proceedings of the National Academy of Sciences (2024). DOI: 10.1073/pnas.2313823121
HIV-infektion parannuskeinotutkimus on vuosien ajan keskittynyt kahteen lähestymistapaan, jotka tunnetaan nimellä "shokki ja tappaminen" ja "esto ja lukitseminen". Ensimmäinen toimii yhdessä antiretroviraalisen hoidon kanssa aktivoidakseen piilevästi infektoituneita soluja ja tappaakseen ne apoptoosin eli ohjelmoidun solukuoleman kautta, kun taas jälkimmäinen pakottaa infektoituneet solut syvään piilevään tilaan, josta ne eivät voi aktivoitua uudelleen itse.
Näitä tekniikoita koskeva tutkimus on perinteisesti keskittynyt T-soluiksi kutsuttuihin valkosoluihin, jotka ovat HIV-infektion ensisijainen kohde. Latenttivarastot koostuvat kuitenkin muustakin kuin vain T-soluista; itse asiassa ne sisältävät kymmeniä erilaisia solutyyppejä, joilla jokaisella on omat ainutlaatuiset HIV-geenien ilmentymismallinsa.
”Solujen monimuotoisuus on valtava, jopa yhden solulinjan sisällä”, sanoo mikrobiologian apulaisprofessori ja artikkelin kirjoittaja Collin Kieffer. ”Vasteen vaihtelevuus näissä reservuaareissa kasvaa jokaisen uuden solutyypin myötä.”
Kiefferin laboratoriossa työskentelevä jatko-opiskelija Alexandra Blanco halusi tutkia solutyyppejä, jotka olivat jääneet huomaamatta perinteisessä HIV-tutkimuksessa. Keskittyen myeloidisoluihin hän loi kloonikirjaston, joka sisälsi 70 latenttisesti infektoituneiden monosyyttien populaatiota. Blanco analysoi sitten kloonipopulaatiot ja niiden vasteet aktivaatioon. Vasteet vaihtelivat suuresti, mikä korosti suurta monimuotoisuutta yhden solutyypin sisällä.
Tämä havainto herätti uuden kysymyksen: reagoivatko eri solutyypit todella eri tavoin HIV-latenssihoitoihin? Heidän löydöksensä osoittivatkin, että jotkut HIV-latenssihoidot voivat edistää latenssivaihetta T-soluissa ja monosyyteissä, kun taas ne voivat kääntää latenssivaiheen makrofageissa.
"Kaikki kehon solut eivät ole samanlaisia", Kieffer sanoi. "Joten on järkevää, etteivät kaikki tartunnan saaneet solut reagoi virukseen samalla tavalla."
Heidän artikkelissaan korostetaan, että tulevissa HIV-hoidoissa on otettava huomioon kaikki solutyypit ja se, miten kukin solu voisi reagoida mahdollisiin hoitoihin.
Heidän löydöksensä perustuvat entisen Illinoisin biotekniikan professorin Roy Darin tutkimukseen, jonka laboratorio tutki HIV-geenien ilmentymisen heterogeenisyyttä.
"Hän aloitti sen, ja me otimme sen haltuumme ja rakensimme sen nykyiseen muotoonsa", Kieffer sanoi. "Joten yhteistyö todella käynnisti nämä tulokset. Se on muuttunut laboratoriomme uudeksi suunnaksi, ja olemme siitä todella innoissamme."
Blancon analyysin odottamaton lisälöydös paljasti solujen koon ja muodon muutoksia infektion seurauksena, mikä viittaa siihen, että HIV voi muuttaa solujen morfologiaa. Blancon seuraava tavoite on tunnistaa näiden fenotyyppisten muutosten taustalla olevat biologiset mekanismit.
Kieffer ja hänen laboratorionsa jäsenet odottavat myös innolla tulosten toistamista primaarisoluissa, jotka tehtiin enimmäkseen solulinjassa. Tulosten toistaminen ihmisen kaltaisessa mallissa parantaisi tutkimuksen kliinistä merkitystä, Kieffer selitti.
"Haluamme tehdä suurempia seulontoja T-soluissa, monosyyteissä ja makrofageissa tunnistaaksemme potentiaalisia lääkkeitä, jotka saattaisivat toimia kaikissa näissä solutyypeissä", Blanco sanoi. "Saatamme löytää vielä enemmän molekyylejä, jotka eivät käyttäydy solutyypille spesifisesti."
