Uudet julkaisut
"Happea soluille": yksinkertainen implantti auttoi alentamaan sokeritasoja ilman vahvoja lääkkeitä
Viimeksi tarkistettu: 18.08.2025

Kaikki iLive-sisältö tarkistetaan lääketieteellisesti tai se tarkistetaan tosiasiallisen tarkkuuden varmistamiseksi.
Meillä on tiukat hankintaohjeet ja vain linkki hyvämaineisiin mediasivustoihin, akateemisiin tutkimuslaitoksiin ja mahdollisuuksien mukaan lääketieteellisesti vertaisarvioituihin tutkimuksiin. Huomaa, että suluissa ([1], [2] jne.) Olevat numerot ovat napsautettavia linkkejä näihin tutkimuksiin.
Jos sinusta tuntuu, että jokin sisältö on virheellinen, vanhentunut tai muuten kyseenalainen, valitse se ja paina Ctrl + Enter.
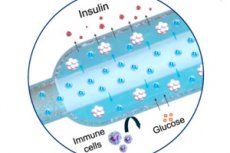
Nature Communications -lehdessä kuvattiin uusi tyypin 1 diabeteksen hoitoon tarkoitettu ”happi”-implantti: kompakti sähkökemiallinen happigeneraattori (iEOG) syöttää jatkuvasti happea makrokapseliin, jossa on insuliinia erittäviä soluja. Tämä järjestelmä mahdollistaa eristettyjen saarekkeiden tiiviin pakkautumisen (jopa 60 000 IEQ/ml) ja ylläpitää niiden elinkykyisyyttä ja eritystä jopa alhaisissa happiolosuhteissa. Diabetesta sairastavilla rotilla ihon alle istutettu laite piti normaalin sokeritason jopa kolme kuukautta – ilman immunosuppressiota. Kontrollirotilla, joilla ei ollut happea, pysyi hyperglykeemisenä.
Tausta
- Tekninen ongelma on pääasiallisesti happi. Heti kun solut "piilotetaan" kalvon taakse ja laite asetetaan ihon alle (joka on kätevästi ja helposti poistettavissa), niiltä puuttuu happea: diffuusio kalvon läpi ja huonosti verisuonitetussa paikassa ei vastaa "ahneiden" saarekkeiden tarpeisiin. Tästä johtuu ennenaikainen kuolema, heikko työ ja tarve ohentaa siemennestettä huomattavasti – muuten kapselista tulee valtava.
- Miksi se on fyysisesti niin vaikeaa? Happi kulkee kudosten läpi vain hyvin lyhyitä matkoja, eikä kapseloiduilla soluilla ole omia verisuonia – ensimmäisten kuukausien ajan ne elävät vain passiivisen diffuusion ansiosta. Materiaalien paksuuntuminen tai solujen "tiivistyminen" siirtää kapselin keskustan nopeasti hypoksiaan.
- Mitä olet kokeillut aiemmin?
- He tekivät hapella täytettäviä makrolaitteita (esimerkiksi βAir): niiden sisällä on säiliö, jota täydennetään hapella päivittäin; siitä on tehty prekliinisiä ja varhaisia kliinisiä tutkimuksia. Se toimii, mutta on potilaalle työlästä.
- Kemiallisia happidonoreita ja "kantaja"materiaaleja (perfluoriyhdisteitä) kokeiltiin: ne auttavat, mutta antavat lyhyen ja vaikeasti hallittavan vaikutuksen. Myös "ilma"-kehyksiä ilmestyi happidioksidin kulkeutumisen nopeuttamiseksi geelin paksuuteen.
- Kapselit itsessään ja implantaatiokohdat (ohuet kalvot, prevaskularisaatio) paranivat, mutta ilman ulkoista O₂-lähdettä ne törmäävät edelleen solutiheysrajoihin.
- Minkä aukon palapelissä uusi työ täyttää? Nature Communicationsin kirjoittajat osoittavat jatkuvan hapen syötön minigeneraattorista suoraan makrokapselointijärjestelmän sisällä: laite ottaa vettä kudoksista ja vapauttaa sähkökemiallisesti happea, joka "hengittää" tasaisesti solukapselin läpi. Ajatuksena on antaa kapselille "oma akvaariokompressori", jotta se voi pakata enemmän soluja ja silti pitää ne elossa ja toiminnassa – jopa ihonalaisessa, ei kovin "hapekkaassa" paikassa.
Miksi tämä on ylipäätään tarpeen?
Saareke- tai beetasolujen siirto on yksi lupaavimmista tavoista löytää tyypin 1 diabetekselle "toiminnallinen parannuskeino". Mutta on olemassa kaksi suurta estettä:
- Immuniteetti - vaatii yleensä elinikäistä immunosuppressiivista lääkitystä;
- Hapenpuute – immuunijärjestelmää suojaavat kapselit eristävät samanaikaisesti solujen yhteyden verisuoniin, ja happihapoista ahneet beetasolut "tukahtuvat" nopeasti. Uusi tutkimus osuu toiseen esteeseen: se antaa kapselille oman, kontrolloidun happilähteen.
Miten implantti toimii
- Kaksi osaa. Titaanikotelossa on mini-happigeneraattori (iEOG), joka erottaa vettä kudosnesteestä ja vapauttaa happea elektrolyysin avulla; sen vieressä on ohut lineaarinen kapseli, jossa on soluja (samanlainen kuin pitkä "makkara"), jonka läpi kulkee kaasua läpäisevä putki: happi imeytyy tasaisesti koko kapselin pituudelle. Solujen ja kudosten välissä on puoliläpäisevä kalvo (elektrolinkous + alginaatti): glukoosi ja insuliini kulkevat läpi, immuunisolut eivät.
- Mitat: iEOG:n toinen versio on halkaisijaltaan 13 mm ja paksuudeltaan 3,1 mm, ja se painaa noin 2 g. Kapseliin yhdistettynä tällainen järjestelmä voidaan asettaa ja poistaa pienen viillon kautta, mikä on turvallisuuden kannalta tärkeää.
- Tuottavuus. Generaattori tuottaa ~1,9–2,3 cm³ O₂/h ja ylläpitää määritettyä virtausta kuukausia ja jopa vuosia (pitkäaikaiskokeissa suolaliuoksessa – jopa 2,5 vuotta), ja rotille implantoinnin jälkeen tämä taso säilyi. Tällainen virtaus on laskettu kattamaan satojen tuhansien saarekeekvivalenttien tarpeet – suuruusluokkaa, jonka ihminen tarvitsee.
Mitä kokeet osoittivat
- In vitro: 1 %:n O₂-pitoisuudessa (vaikea hypoksia) hapetus ylläpiti elinkykyisyyttä ja eritystä INS-1-aggregaateissa ja ihmisen saarekkeissa, jotka olivat pakattu erittäin tiheäksi kerrokseksi (60 000 IEQ/ml).
- In vivo (rotat). Allogeeniseen diabetesmalliin ihon alle tehdyn implantaation jälkeen iEOG-järjestelmä normalisoi glykemiaa jopa 3 kuukaudeksi ilman immunosuppressiota; happea vailla olevilla laitteilla ei ollut vaikutusta. Generaattorin ympärillä oleva histologinen tutkimus ei osoittanut merkittäviä haittavaikutuksia.
Miksi tämä on tärkeää klinikalle?
- Askel kohti ”realistisia ulottuvuuksia”. Jotta aikuiselle voitaisiin antaa 300–770 000 IEQ:n annos, kapselin on oltava tiiviisti pakattu – tätä on aina rajoittanut happi. Hallittu O₂-syöttö ”poistaa katon” tiheydeltä ja antaa mahdollisuuden tehdä laitteesta riittävän kompakti todellista implantaatiota varten.
- Lisäksi kätevyys. Aiemmin kokeilimme kemiallisia happidonoreita (peroksideja) – ne eivät tehoa pitkään eivätkä ole hallittavissa, sekä happisäiliöitä, jotka "täytetään" päivittäin ihon kautta – kömpelöitä ja epämukavia. Näissä happea toimitetaan jatkuvasti ja mitattuina annoksina ilman injektioita.
Vaikuttavia teknisiä yksityiskohtia
- Veden lähde on kudos. iEOG imee kudosnesteen höyryä huokoisen "ikkunan" läpi, ja sitten klassista kalvoelektrodikokoonpanoa (MEA) ja 1,4–1,8 V jännitettä käytetään veden erottamiseen H₂:ksi ja O₂:ksi; kaasut poistetaan eri kanavien kautta.
- Kestävyys. Kolme suolaliuokseen upotettua laitetta toimi tasavirralla 11 kuukautta, 2 vuotta ja 2,5 vuotta ilman happivirtauksen aiheuttamaa heikkenemistä; immuunipuutteisille ja immuunipuutteisille rotille implantoinnin jälkeen suorituskyky säilyi.
Rajoitukset ja "mitä seuraavaksi"
Tämä on vielä prekliinistä vaihetta: rotat, suuri kapselin tiheys, hapen saanti – kaikki on hienoa, mutta tärkeät testit ovat vielä edessä:
- skaalaus ihmisille tarkoitettuihin annoksiin ja aikaväleihin;
- sähkökemistien luotettavuus ja virransyöttö ihmiskehossa vuosien ajan (virtalähteen arkkitehtuuria ei ole yksityiskohtaisesti kuvattu artikkelissa);
- kapseleiden ympärillä olevan fibroosin minimointi ja diffuusion vakaus;
- testausta beeta-kantasoluilla ja ihmisiä lähempänä olevilla malleilla. Kirjoittajat vertaavat ratkaisuaan avoimesti aiempiin lähestymistapoihin ja asettavat sen alustaksi kliinisesti käännettävissä oleville kapseleille.
Johtopäätös
Jotta siirretyt beetasolut voisivat elää ja toimia ilman immunosuppressantteja, niiden on hengitettävä. Cornellin ja kumppaneiden tiimi osoitti, että lineaariseen kapseliin rakennettu mini-happigeneraattori voi "ruokkia" soluja hapella riittävän kauan ja tasaisesti, jotta ne kestävät suurta tiheyttä ja vähentävät sokeria jopa ihonalaisessa paikassa. Klinikka on vielä kaukana, mutta tekninen logiikka on yksinkertainen ja kaunis – antaa soluille ilmaa sieltä, missä sitä on pulaa.
